
下列物质中,化学键类型完全相同的是
A.CaBr2与HCl B.MgCl2与Na2S
C.KOH与NaCl D.H2O与NaCl
 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源:2013-2014山东省青岛市高三第二次模拟考试理综化学试卷(解析版) 题型:推断题
(12分)【化学——有机化学基础】
某研究小组以甲苯为主要原料,合成医药中间体F和Z。
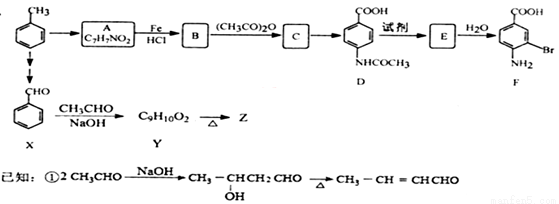
②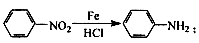 苯胺中氨基易被氧化。
苯胺中氨基易被氧化。
请回答下列问题:
(1)有机物A的结构简式为 。
(2)下列有关F的说法正确的是 。
a.分子式是C7H7NO2Br b.能形成内盐
c.能发生酯化反应和缩聚反应 d.1 mol的F最多可以和2 mol NaOH反应
(3)B→C的化学方程式是 。在合成F的过程中,B→C步骤不能省略,理由是 。
(4)写出同时符合下列条件的Z的同分异构体(不含Z,不考虑立体异构)。
①含有苯环结构 ②与Z含有相同官能团
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高二化学试卷(解析版) 题型:简答题
(10分) 某有机化合物A的结构简式如下:
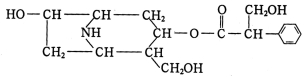
请回答下列问题:
(1)A的分子式是。CH2OH COOH Na
(2)A在NaOH溶液中加热反应得到B和C,C分子中含有苯环。B的结构简式是 。
(3)室温下,C用稀盐酸酸化得到E,E的结构简式是 。
(4)在下列物质中,能与E发生化学反应的是(填写序号)。
①溴水 ②FeCl3溶液 ③Na2CO3溶液④丁烷
(5)写出在铜作催化剂时,E与氧气反应的化学方程式:
。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高二化学试卷(解析版) 题型:选择题
下列叙述错误的是
A.乙烯和苯都能使溴水褪色,褪色的原理相同
B.淀粉、油脂、蛋白质都能水解,但水解产物不同
C.乙酸乙酯中的少量乙酸可用饱和Na2CO3溶液除去
D.煤油可由石油分馏获得,可用作燃料和保存少量金属钠
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高一化学试卷(解析版) 题型:填空题
(6分)下图中A、B、C、D是常见的普通玻璃试剂瓶。请把下列试剂的序号填写在适合盛放的试剂瓶下面的括号内:
a.浓硫酸 b.碳酸钠溶液 c.铝片 d.浓硝酸 e.氢氧化钠溶液 f.二氧化锰
A | B | C | D |
|
|
|
|
( ) | ( ) | ( ) | ( ) |
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省潍坊市下学期期中考试高一化学试卷(解析版) 题型:选择题
下列有关周期表的叙述中正确的是
A.碱土金属元素是指ⅡA族的所有元素
B.除第一周期外,其他周期均有18种元素
C.过渡元素都是副族元素
D.主族元素的原子,半径越大,越容易得到电子
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三第三次模拟考试理综化学试卷(解析版) 题型:推断题
(12分)【化学——有机化学基础】
化合物F是合成新农药的重要中间体。

以化合物A(分子式为C7H7Cl)为原料合成化合物F的工艺流程如下:
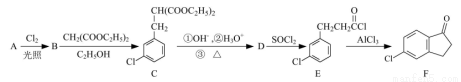
(1)反应A→B的化学方程式为_______。
(2)D的分子式为_______。
(3)化合物F中含氧官能团的名称为_________,B→C的反应类型为_______。
(4) E→F的转化中,会生成一种含有五元环的副产物且与F互为同分异构体,其结构简式为_______ 。
(5)反应C→D过程中,D可能发生水解,可用于检验的试剂是 _______。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省淄博市高三二模理综化学试卷(解析版) 题型:填空题
(17分)降低太气中CO2含量及有效开发利用CO2,是科学家研究的重要课题。
(1)将燃煤废气中的CO2转化为二甲醚的反应原理为:
2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g) △H=-122.4kJ·mol-1
CH3OCH3(g)+3H2O(g) △H=-122.4kJ·mol-1
①某温度下,将2.0molCO2(g)和6.0molH2(g)充入体积可变的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化如下表所示。
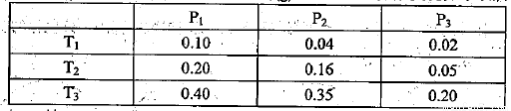
则Pl P3(填“>”“<”或“=”,下同)。若T1、Pl,T3、P3时平衡常数分别为K1、K3,
则K1 K3。T1、Pl时H2的平衡转化率为 。
②一定条件下,t上述反应在密闭容器中达平衡。当仅改变影响反应的一个条件,引起的下列变化能说明平衡一定向正反应方向移动的是____ 。
A.反应物的浓度降低 B.容器内压强增大
C.正反应速率大于逆反应速率 D.化学平衡常数K增大
(2)碳酸氢钾溶液加水稀释,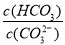 (填“增大”“不变”或“减小”)。用碳酸钾溶液吸收空气中CO2,当溶渡呈中性时,下列关系或说法正确的是 。
(填“增大”“不变”或“减小”)。用碳酸钾溶液吸收空气中CO2,当溶渡呈中性时,下列关系或说法正确的是 。
A.c(K+)=2c(CO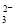 )+c(HCO
)+c(HCO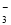 )+c(H2CO3)
)+c(H2CO3)
b.c(HCO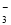 )
)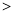 c(CO
c(CO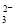 )
)
c.降低温度,c(H+)·c(OH-)不变
(3)向盛有FeCl3溶液的试管中滴加少量碳酸钾溶液,立即产生气体,溶液颜色加深,用激光笔照射能产生丁达尔效应,反应的离子方程式为 。
查看答案和解析>>
科目:高中化学 来源:2013-2014山东省济宁市高一5月质量检测化学试卷(解析版) 题型:选择题
100 mL 2 mol/L H2SO4 与过量Zn粉反应,在一定温度下,为了加快反应速率,但又不影响生成氢气的总量,可以采取的措施是( )
A.加入碳酸钠固体 B.改用18 mol/L的浓H2SO4
C.滴入少量硫酸铜溶液 D.加入硫酸钾溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com