
| A. | 从HF、HCl HBr、HI的酸性递增的事实,推出F、Cl、Br、I的非金属性递增的规律 | |
| B. | Na在氧气中燃烧主要生成Na2O | |
| C. | 第三周期非金属元素含氧酸的酸性从左到右依次减弱 | |
| D. | 元素周期律是元素原子核外电子排布周期性变化的结果 |
分析 A.以酸性强弱判断元素非金属性强弱时,是以最高价氧化物对应水化物的酸性强弱为判断依据的;
B.钠在氧气中燃烧生成过氧化钠;
C.必须指出最高价含氧酸,否则该说法不合理;
D.原子的结构决定着元素的性质,元素周期律是元素原子核外电子排布周期性变化的结果.
解答 解:A.元素非金属性越强,对应的最高价氧化物的水化物的酸性越强,与氢化物的酸性无关,不能根据氢化物酸性强弱判断非金属性,故A错误;
B.Na在空气中缓慢氧化生成Na2O,在氧气中燃烧生成Na2O2,故B错误;
C.第三周期非金属元素的最高价含氧酸的酸性从左到右依次减弱,没有指出最高价,该说法不合理,故C错误;
D.原子的结构决定着元素的性质,最外层电子的排布呈规律性变化,则性质呈周期性变化,即元素周期律是元素原子核外电子排布周期性变化的结果,故D正确;
故选D.
点评 本题原子结构与元素周期律的应用,题目难度不大,注意把握元素周期律的递变性和相似性,明确元素周期律的内容为解答关键,试题有利于提高学生的分析能力及综合应用能力.


 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案 黄冈海淀全程培优测试卷系列答案
黄冈海淀全程培优测试卷系列答案科目:高中化学 来源: 题型:选择题
| A. | 金刚石网状结构中,由共价键形成的碳原子环中,最小的环上有6个碳原子 | |
| B. | 12g石墨中含有σ键的个数为2NA (NA表示阿伏伽德罗常数) | |
| C. | 氯化铯晶体中,每个Cs+周围紧邻8个Cl- | |
| D. | 干冰晶体中,每个CO2分子周围紧邻12个CO2分子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
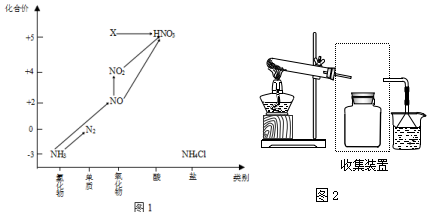
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯气溶于水:Cl2+H2O═2H++Cl-+ClO- | |
| B. | NH4HCO3溶液和足量氢氧化钠溶液反应:NH4++OH-═NH3•H2O | |
| C. | 向FeBr2溶液中通入少量氯气:Fe2++Cl2═Fe3++2Cl- | |
| D. | 氯气与Na2SO3溶液反应:Cl2+SO32-+H2O═SO42-+2Cl-+2H+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 Ⅰ.铁及铁的化合物应用广泛,如FeCl3可用作印刷电路铜版腐蚀剂和外伤止血剂等.
Ⅰ.铁及铁的化合物应用广泛,如FeCl3可用作印刷电路铜版腐蚀剂和外伤止血剂等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所有卤代烃都难溶于水,且都是密度比水大的液体 | |
| B. | 所有卤代烃都是通过取代反应制得 | |
| C. | 卤代烃可用作制冷剂、灭火剂 | |
| D. | 卤代烃都是良好的有机溶剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 时间/min | 1 | 2 | 3 | 4 | 5 |
| 氢气体积/mL | 50 | 120 | 232 | 290 | 310 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com