
可逆反应A(g)+B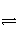
 C(g)+D,反应式中A和C都是无色气体。当反应达到平衡时,下列叙述错误的是( )
C(g)+D,反应式中A和C都是无色气体。当反应达到平衡时,下列叙述错误的是( )
A.若增大A的浓度,平衡体系颜色加深,则说明D是有颜色的气体
B.若升高温度,C的百分含量减小,则说明正反应为放热反应
C.若增大压强平衡不发生移动,则说明B和D一定都是气体
D.如果B是气体,则增大A的浓度会使B的转化率增大
科目:高中化学 来源: 题型:
今有三个氧化还原反应: ①2FeCl3+2KI===2FeCl2+2KCl+I2
②2FeCl2+Cl2===2FeCl3 ③2KMnO4+16HCl===2KCl+2MnCl2+5Cl2↑+8H2O
若某溶液中有Fe2+、I-、Cl-共存,要除去I-而不氧化Fe2+和Cl-,则可加入的试剂是( )
A.Cl2 B.KMnO4 C.FeCl3 D.HCl
查看答案和解析>>
科目:高中化学 来源: 题型:
磁性纳米颗粒稳定、容易生产且用途广泛,是临床诊断、生物技术和环境化学领域多种潜在应用的有力工具。水热法制备Fe3O4纳米颗粒的反应是3Fe2++2S2O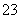 +O2+xOH-===Fe3O4+S4O
+O2+xOH-===Fe3O4+S4O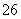 +2H2O。请回答下列问题。
+2H2O。请回答下列问题。
(1)水热法制备Fe3O4纳米颗粒的反应中,还原剂是_________。(2)反应的化学方程式中x=______。
(3)每生成1 mol Fe3O4,反应转移的电子为________mol,被Fe2+还原的O2的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知可逆反应:M(g)+N(g)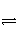
 P(g)+Q(g) ΔH>0,请回答下列问题:
P(g)+Q(g) ΔH>0,请回答下列问题:
(1)在某温度下,反应物的起始浓度分别为:c0(M)=1 mol·L-1,c0(N)=2.4 mol·L-1;达到平衡后,M的转化率为60%,此时N的转化率为________;
(2)若反应温度升高,M的转化率________(填“增大”、“减小”或“不变”);
(3)若反应温度不变,反应物的起始浓度分别为:c0(M)=4 mol·L-1,c0(N)=a mol·L-1;达到平衡后,[P]=2 mol·L-1,a=________;
(4)若反应温度不变,反应物的起始浓度为:c0(M)=c0(N)=b mol·L-1,达到平衡后,M的转化率为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
对于xA(g)+yB(g)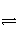
 zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法中正确的是( )
zC(g)+wD(g)的平衡体系,当升高温度时,体系的平均相对分子质量从26变为29,则下列说法中正确的是( )
A.若x+y>z+w,正反应是放热反应
B.若x+y>z+w,正反应是吸热反应
C.若x+y<z+w,逆反应是放热反应
D.若x+y>z+w,逆反应是吸热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
COCl2(g)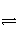
 CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
CO(g)+Cl2(g) ΔH>0。当反应达到平衡时,下列措施:①升温 ②恒容通入惰性气体 ③增加CO的浓度 ④减压 ⑤加催化剂 ⑥恒压通入惰性气体,能提高COCl2转化率的是( )
A.①②④ B.①④⑥ C.②③⑤ D.③⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
对于可逆反应mA(g)+nB(s)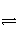
 pC(g)+qD(g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如下图,下列说法正确的是( )
pC(g)+qD(g),反应过程中,其他条件不变时,产物D的物质的量分数D%与温度T或压强p的关系如下图,下列说法正确的是( )
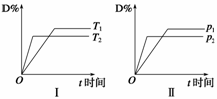
A.降温可使化学平衡向正反应方向移动
B.使用合适的催化剂可使D%有所增加
C.化学方程式中化学计量数:m>p+q
D.B的颗粒越小,正反应速率越快,有利于平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
只改变一个影响因素,平衡常数K与化学平衡移动的关系叙述错误的是 )。
A.K值不变,平衡可能移动
B.K值变化,平衡一定移动
C.平衡移动,K值可能不变
D.平衡移动,K值一定变化
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com