
高温下,某反应达平衡,平衡常数K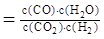 。恒容时,温度升高
。恒容时,温度升高 浓度减小。下列说法正确的是( )
浓度减小。下列说法正确的是( )
| A.该反应的焓变为正值 |
B.恒温恒容下,增大压强 浓度一定减小 浓度一定减小 |
| C.升高温度,逆反应速率减小 |
D.该反应化学方程式为  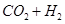 |
A
解析试题分析:化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,所以根据平衡常数的表达式可知,该反应的方程式是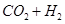

 ,D不正确;恒容时,温度升高
,D不正确;恒容时,温度升高 浓度减小,说明升高温度,平衡向正反应方向移动,因此正反应是吸热反应,A正确;反应前后体积不变,压强不能影响平衡状态,B不正确;升高温度正逆反应速率都是增大的,C不正确,答案选A。
浓度减小,说明升高温度,平衡向正反应方向移动,因此正反应是吸热反应,A正确;反应前后体积不变,压强不能影响平衡状态,B不正确;升高温度正逆反应速率都是增大的,C不正确,答案选A。
考点:考查平衡常数的有关由于、外界条件对平衡状态的影响等
点评:由于压强对反应速率或平衡状态的影响是通过改变浓度来实现的,所以压强对反应速率或平衡状态的影响在判断时需要注意压强的变化是否能引起浓度的变化,否则反应速率或平衡状态是有可能不变的,需要具体问题具体分析,灵活运用,且不可生搬硬套。


科目:高中化学 来源: 题型:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| c(CO)?c(H2O) |
| c(CO2)?c(H2) |
| A、该反应的焓变为负值 | |||
B、该反应化学方程式为CO+H2O
| |||
| C、恒温恒容下,充入CO2,H2浓度一定减小 | |||
| D、升高温度,逆反应速率减小 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com