

| ������ | Fe��OH��3 | Al��OH��3 | Cu��OH��2 |
| ��ʼ���� | 1.1 | 4.0 | 5.4 |
| ��ȫ���� | 3.2 | 5.2 | 6.7 |
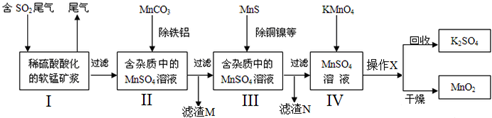
���� �����̿�֪����ϡ���ᡢ�������⣬ֻ��Au��Pt����Ӧ������ΪAu��Pt��Cu��Al��Fe��ת��Ϊ���������ӣ�Ȼ���NaOH��Һ����pHΪ[5.2��5.4����ֻ��ͭ��������Һ�У�����Ũ���õ�����ͭ���壬������aΪ��������������������Ϊ�õ���������������������ܽ����Al��Ӧ��������Һ���ᾧ�õ����壬�Դ������
��� �⣺�����̿�֪����ϡ���ᡢ�������⣬ֻ��Au��Pt����Ӧ������ΪAu��Pt��Cu��Al��Fe��ת��Ϊ���������ӣ�Ȼ���NaOH��Һ����pHΪ[5.2��5.4����ֻ��ͭ��������Һ�У�����Ũ���õ�����ͭ���壬������aΪ��������������������Ϊ�õ���������������������ܽ����Al��Ӧ��������Һ���ᾧ�õ����壬
��1��Cu��ϡ�����H2O2�Ļ��Һ��Ӧ�Ļ�ѧ����ʽΪCu+H2O2+H2SO4=CuSO4+2H2O���ʴ�Ϊ��Cu+H2O2+H2SO4=CuSO4+2H2O��
��2���ɱ����е����ݿ�֪����֤ͭ���Ӳ�ת��Ϊ��������pHΪ[5.2��5.4�����ʴ�Ϊ��[5.2��5.4����
��3������III�У�����Ũ����Ҫ�IJ��������в��������ƾ��ơ��ձ����ʴ�Ϊ�����������ƾ��ơ��ձ���
��4��������������֪������aΪ��������������������Ϊ�õ���������������������ܽ����Al��Ӧ��������Һ���ᾧ�õ����壬����������ʴ�Ϊ���ң�
��5����Cu2++H2Y2-=CuY2-+2H+���ζ����յ㣬ƽ������EDTA��Һ12.00mL����CuSO4.5H2O����Ĵ�����$\frac{0.012L��bg/mol��\frac{100}{20}��250g/mol}{ag}$��100%=$\frac{15b}{a}$��100%��
�ʴ�Ϊ��$\frac{15b}{a}$��100%��
���� ���⿼�������Ʊ�ʵ��ʵ�����Ƽ����ʺ����IJⶨ��Ϊ��Ƶ���㣬�����Ʊ�ʵ�����̼������ķ�ӦΪ���Ĺؼ������ط�����ʵ�顢���������Ŀ��飬��Ŀ�Ѷ��еȣ�


 �ŵ������ϵ�д�
�ŵ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��NO${\;}_{3}^{-}$��AlO${\;}_{2}^{-}$��SO${\;}_{4}^{2-}$ | B�� | Na+��Al3+��NO${\;}_{3}^{-}$��SO${\;}_{4}^{2-}$ | ||
| C�� | K+��Cl-��AlO${\;}_{2}^{-}$��CO${\;}_{3}^{2-}$ | D�� | Na+��Mg2+��Cl-��HCO${\;}_{3}^{-}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��3 | B�� | 1��2 | C�� | 1��1 | D�� | 2��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ������������������������ԭ��Ӧ�������� | |
| B�� | �廯������ȶ��Աȵ⻯������ȶ��Բ� | |
| C�� | KI������Һ����ˮ��Ӧ��֤����Ľ����Աȵ�Ľ���ǿ | |
| D�� | I2O5��Br2O5��ˮ��Ӧ���ɶ�Ӧ�ĸ�±�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����̼ԭ���������ӣ��������ۡ��е����� | |
| B�� | ���л����У�̼ԭ��ͨ���ĸ����ۼ�������ԭ�ӽ�� | |
| C�� | ���顢��ϩ����ʹ���Ը��������Һ��ɫ | |
| D�� | �����ڹ���������������ȡ����Ӧ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
 ��ͼ����ԭ�����м���������̿�ۣ���Ͼ��Ⱥ������ڱ���NaCl��Һ��ʪ���ľ�֧�Թ��У�������Ƥ����Լ10���Ӻ�ֹˮ�У��۲쵽������ˮ���������Դ˵绯ѧ��ʴ���������ķ�����ȷ���ǣ�������
��ͼ����ԭ�����м���������̿�ۣ���Ͼ��Ⱥ������ڱ���NaCl��Һ��ʪ���ľ�֧�Թ��У�������Ƥ����Լ10���Ӻ�ֹˮ�У��۲쵽������ˮ���������Դ˵绯ѧ��ʴ���������ķ�����ȷ���ǣ�������| A�� | ���������� | B�� | ̿�۱����� | C�� | ������������ʴ | D�� | ���������ⸯʴ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com