
分析 由2Fe3++2I-=2Fe2++I2;2Fe2++Br2=2Br-+2Fe3+可知,还原性强弱顺序是:I->Fe2+>Br-,向溶液中通入氯气,氯气先和碘离子反应,然后再和亚铁离子反应,最后再和溴离子反应,结合碘化亚铁、溴化亚铁的物质的量及氯气的物质的量、电子守恒进行分析、计算即可.
解答 解:(1)向含有1mol FeI2和2mol FeBr2的溶液中通入2mol Cl2,先发生反应2I-+Cl2=I2+2Cl-,2mol碘离子完全反应需要氯气1mol,然后发生反应Cl2+2Fe 2+=2Cl-+2Fe3+,1mol氯气反应需要亚铁离子的物质的量是2mol,溶液中含有3mol亚铁离子,参加反应的亚铁离子的物质的量是2mol,所以溶液中还剩余亚铁离子1mol,所以被氧化的离子是2molI-、2molFe 2+,
故答案为:I-、Fe 2+;2mol、2mol;
(2)向含有1mol FeI2和2mol FeBr2的溶液中通入3mol Cl2,先发生反应2I-+Cl2=I2+2Cl-,2mol碘离子完全反应需要氯气1mol,然后发生反应Cl2+2Fe 2+=2Cl-+2Fe3+,溶液中含有3mol亚铁离子,亚铁离子完全被氧化,则需要氯气的物质的量是1.5mol,最后发生2Br-+Cl2=Br2+2Cl-,溴离子的物质的量是3mol,则需要氯气的物质的量是1.5mol,实际上还有0.5mol氯气,则被氧化的溴离子的物质的量是1mol,所以溶液中还剩下0.5mol溴离子,则被氧化的离子及物质的量为:2molI-、3molFe2+、1molBr-,对应的氧化产物分别是1molI2、3molFe 3+、0.5molBr2,反应的总离子方程式为:6Fe3++4I-+2Br-+6 Cl2═6Fe3++2I2+Br2+12Cl-,
故答案为:I-、Fe2+、Br-; I2 1 mol、Fe3+ 3 mol、Br2 0.5 mol;6Fe3++4I-+2Br-+6 Cl2═6Fe3++2I2+Br2+12Cl-;
(3)a mol FeI2和b mol FeBr2的溶液中总共含有(a+b)molFe2+、2amolI-、2bBr-,根据反应方程式:2I-+Cl2=I2+2Cl-、Cl2+2Fe2+=2Cl-+2Fe3+、2Br-+Cl2=Br2+2Cl-可知,消耗的氯气的物质的量为c=$\frac{1}{2}$×(a+b+2a+2b)mol=$\frac{3(a+b)}{2}$mol,
故答案为:$\frac{3(a+b)}{2}$.
点评 本题考查氧化还原反应计算,为高频考点,明确还原性的强弱、氧化还原反应的先后顺序是解答本题的关键,侧重分析与计算能力的考查,题目难度中等.


科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
 ,B 同周期第一电离能最小的主族元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题:
,B 同周期第一电离能最小的主族元素,C的最外层有三个成单电子,E的外围电子排布式为3d64s2.回答下列问题: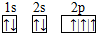 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com