
【题目】实验室常用碱性溶液吸收多余的氯气,防止污染环境。若某一次兴趣小组实验中将多余的氯气用100 mL 2.00 mol·L-1的NaOH溶液恰好完全吸收。分析吸收液测得ClO-和![]() 的物质的量浓度之比为5∶1。请回答:
的物质的量浓度之比为5∶1。请回答:
(1)吸收的氯气的物质的量为____mol。
(2)若不考虑吸收前后溶液体积变化,则吸收液中Cl-的物质的量浓度为________。
【答案】0.100 1.25 mol·L-1
【解析】
(1)根据题意,NaOH溶液吸收Cl2时发生反应:Cl2+2NaOH![]() NaCl+NaClO+H2O和3Cl2+6NaOH
NaCl+NaClO+H2O和3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,从化学方程式来看,参加反应的氯气的量始终是参加反应的NaOH的量的一半;
5NaCl+NaClO3+3H2O,从化学方程式来看,参加反应的氯气的量始终是参加反应的NaOH的量的一半;
(2) 若吸收液中ClO-和ClO3-的物质的量浓度之比5∶1,从得失电子守恒的观点来看,则三种微粒的物质的量浓度之比c(Cl-)∶c(ClO-)∶c(![]() )=10∶5∶1,根据Na、氯原子守恒求算。
)=10∶5∶1,根据Na、氯原子守恒求算。
(1)根据题意,NaOH溶液吸收Cl2时发生反应:Cl2+2NaOH![]() NaCl+NaClO+H2O和3Cl2+6NaOH
NaCl+NaClO+H2O和3Cl2+6NaOH![]() 5NaCl+NaClO3+3H2O,从化学方程式来看,参加反应的氯气的量始终是参加反应的NaOH的量的一半,所以吸收的氯气的物质的量为2mol/L×0.1L÷2=0.100 mol;
5NaCl+NaClO3+3H2O,从化学方程式来看,参加反应的氯气的量始终是参加反应的NaOH的量的一半,所以吸收的氯气的物质的量为2mol/L×0.1L÷2=0.100 mol;
(2) 若吸收液中ClO-和ClO3-的物质的量浓度之比5∶1,从得失电子守恒的观点来看,则三种微粒的物质的量浓度之比c(Cl-)∶c(ClO-)∶c(![]() )=10∶5∶1,根据Na、氯原子守恒,c(Cl-)+c(ClO-)+c(
)=10∶5∶1,根据Na、氯原子守恒,c(Cl-)+c(ClO-)+c(![]() )= 2mol/L,可知c(Cl-)=1.25 mol·L-1。
)= 2mol/L,可知c(Cl-)=1.25 mol·L-1。


科目:高中化学 来源: 题型:
【题目】现有以下物质:①CCl4 ②Ag ③氨水 ④SO2 ⑤小苏打固体 ⑥Fe(OH)3胶体 ⑦FeCl3溶液
(1)以上物质属于电解质的是_____,属于非电解质的是_____;(填序号)
(2)请写出将少量SO2通入小苏打溶液中反应的离子方程式:_____;
(3)鉴别胶体和溶液最简单有效的物理方法是_____;分离胶体和溶液常用的物理方法是_____;
(4)写出实验室制备NH3的化学方程式_____;为了收集干燥的NH3,下面可选用_____作干燥剂。(填字母序号)
A.浓硫酸 B.碱石灰 C.无水硫酸铜
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲用下列装置制取纯净FeCl3固体。其中A是Cl2的发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网,F为干燥的空广口瓶,烧杯G为尾气吸收装置。
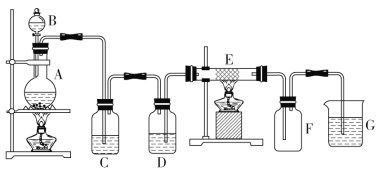
试回答:
(1)该装置中有一明显错误是____________(填字母)。
(2)D中所装试剂为_____________,C装置的作用是___________________。
(3)A中发生反应的化学方程式是__________________,G中发生反应的离子方程式是________________。
(4)若用100mL 12mol/L盐酸与足量MnO2充分反应,生成的Cl2体积(标准状况)________(填“大于”“小于”或“等于”)6.72 L。
(5)用所制取的FeCl3固体制成Fe(OH)3胶体,区分胶体和溶液常用________,分离胶体和溶液常用的方法叫_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.液态HCl不导电,所以HCl是非电解质
B.NH3、CO2的水溶液能导电,所以NH3、CO2是电解质
C.铜、石墨均能导电,所以它们都是电解质
D.蔗糖在水溶液中或熔融时均不导电,所以是非电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有一铁的氧化物样品,用140 mL 5 mol·L-1的盐酸恰好完全溶解,所得溶液还能与通入的0.56 L氯气(标准状况)反应,使Fe2+全部转化为Fe3+,则此氧化物为
A.Fe2O3B.Fe3O4C.Fe4O5D.Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中A~H均为中学化学中常见的物质,A、B、H为气体,反应①是重要的工业反应,它们之间有如下转化关系(反应中生成的水已略去)。
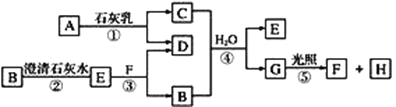
请回答以下问题:
(1)B是________,D是________,G是________,H是________(填化学式)。
(2)工业上常利用反应①制取漂白粉,该反应的化学方程式:_____________________,漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________________。
(3)A中元素的原子结构示意图为________________。
(4)上述反应中属于氧化还原反应的是_________(填写序号)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用NaI溶液中通入少量Cl2得到含碘废液,再利用含碘废液获取NaI固体,实验流程如下:

已知反应②:2I﹣+2Cu2++![]() +H2O
+H2O![]() 2CuI↓+
2CuI↓+![]() +2H+。
+2H+。
回答下列问题:
(1)过滤实验所需要的玻璃仪器有普通漏斗、烧杯、_____________。
(2)反应③中CuI被氧化,还原产物只有NO2,该反应的化学方程式为_________________。当有95.5 g CuI参与反应,则需要标况下______________L的O2才能将生成的NO2在水中完全转化为硝酸。
(3)化合物B中含两种元素,铁原子与另一种元素原子的物质的量之比为3∶8,则化合物B的化学式为_____________。
(4)反应⑤中生成黑色固体和无色气体,黑色固体的俗称为磁性氧化铁,则反应⑤的化学方程式为______。
(5)将足量的Cl2通入含12 g NaI的溶液中,一段时间后把溶液蒸干得到固体的质量为_________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2与足量碳在体积可变的恒压密闭容器中反应:C(s)+CO2(g)![]() 2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g)。平衡时,体系中气体体积分数与温度的关系如下图所示:
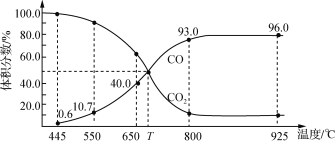
下列说法正确的是
A.650 ℃时,反应达平衡后CO2的转化率为25.0%
B.550 ℃时,若充入惰性气体,υ(正)、υ(逆)均减小,平衡不移动
C.T ℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D.925 ℃时,此反应的平衡常数K=2304,保持温度不变,若缩小体积,K值将变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生用如图所示装置进行化学反应X+2Y![]() 2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到U形管中液面甲处降、乙处升。关于该反应的下列叙述中正确的是
2Z能量变化情况的研究。当往试管中滴加试剂Y时,看到U形管中液面甲处降、乙处升。关于该反应的下列叙述中正确的是

①该反应为放热反应;②该反应为吸热反应;③生成物的总能量比反应物的总能量更高;④反应物的总能量比生成物的总能量更高;⑤该反应过程可以看成是“贮存“于X、Y内部的部分能量转化为热能而释放出来。
A. ①④⑤ B. ①④ C. ①③ D. ②③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com