
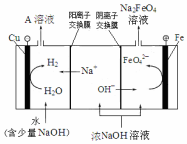
 高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.
高铁酸钾(K2FeO4)是一种新型、高效、多功能水处理剂.分析 (1)①根据n=CV和m=nM来计算;根据配制一定物质的量浓度的溶液的步骤是计算、称量、溶解、移液、洗涤、定容、摇匀来选择使用的仪器;
②依据阳极是铁,故阳极上铁放电生成FeO42-结合碱性环境来写出电极方程式;根据OH-在阳极被消耗,而在阴极会生成来分析;
(2)①CrO2-与FeO42-反应生成Fe(OH)3和CrO42-,根据化合价的升降结合溶液环境可写;
②K2Cr2O7溶液为橙色、Fe3+的溶液为黄色;
③CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-;6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O,依据反应的定量关系和铬元素守恒计算.
解答 解:(1)①所需的NaOH的物质的量n=cV=16mol/L×0.5L=8mol,质量m=nM=8mol×40g/mol=320.0g;根据配制一定物质的量浓度的溶液的步骤是计算、称量、溶解、移液、洗涤、定容、摇匀可知所需的仪器为天平、烧杯、玻璃棒、500mL容量瓶、胶头滴管,其中玻璃仪器有:烧杯、玻璃棒、500mL容量瓶、胶头滴管,
故答案为:320.0;烧杯、玻璃棒、500mL容量瓶、胶头滴管;
②阳极是铁,故阳极上铁放电生成FeO42-,由于是碱性环境,故电极方程式为:Fe-6e-+8OH-=FeO42-+4H2O;在电解时,水电离的H+在阴极放电:2H++2e-=H2↑,c(OH-)增大,Na+通过阳离子交换膜进入阴极区,使阴极区c(NaOH)增大,故NaOH可以循环使用;
故答案为:Fe-6e-+8OH-=FeO42-+4H2O;NaOH溶液;水电离的H+在阴极放电:2H++2e-=H2↑,c(OH-)增大,Na+通过阳离子交换膜进入阴极区,使阴极区c(NaOH)增大,故NaOH可以循环使用;
(2)①CrO2-与FeO42-反应生成Fe(OH)3和CrO42-,离子方程式为:CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-;
故答案为:CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-;
②步骤5中加指示剂,原因是Cr2O72-溶液为橙色,Fe3+溶液为黄色,颜色变化不明显;
故答案为:Cr2O72-溶液为橙色,Fe3+溶液为黄色,颜色变化不明显;
③CrO2-+FeO42-+2H2O=Fe(OH)3↓+CrO42-+OH-;6Fe2++Cr2O72-+14H+═6Fe3++2Cr3++7H2O,得到定量关系为:
2FeO42-~2CrO42-~Cr2O72-~6Fe2+,
2 6
n 0.0300L×0.1000mol/L
n=0.001mol,
100ml溶液中含有0.001mol×$\frac{100mL}{25mL}$=0.004mol,
测定该样品中K2FeO4的质量分数=$\frac{0.004mol×198g/mol}{1.0g}$×100%=79.2%,
故答案为:79.2%.
点评 本题考查了Na2FeO4的制备、化学平衡、溶液的配制以及电极反应的书写,物质含量测定等,需要学生具备扎实的基础,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | Fe2+、SO42-、Fe3+、Cl- | B. | S2-、Cu2+、Na+、Cl- | ||
| C. | H+、SO42-、Cu2+、OH- | D. | Fe2+、H+、Mg2+、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 17g NH3所含的电子数是17NA | |
| B. | 32 g O3中含有氧原子的个数为2NA | |
| C. | 5.6gFe与足量盐酸完全反应,Fe失去的电子数为0.3NA | |
| D. | 标准状况下,11.2 LH2O中含有O-H键的数目为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
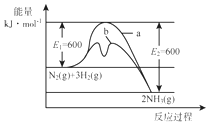 氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法.
氨是氮循环过程中的重要物质,氨的合成是目前普遍使用的人工固氮方法.| 编号 | 温度/K | 反应时间/h | 反应物质的量配比 | 实验目的 |
| ① | 573 | 4 | 1:3 | 实验②和④探究温度对产率的影响 |
| ② | 573 | 4 | 1:4 | |
| ③ | 573 | 3 | 4:1 | 实验②和③探究反应时间对 产率的影响 |
| ④ | 673 | 4 | 1:4 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 工业上利用铝热反应炼铁 | |
| B. | 将Mg、Al用导线连接并插入NaOH溶液中,判断Mg、Al金属性强弱 | |
| C. | 将CO2、SO2分别通入Ba(NO3)2溶液中,前者无明显现象,后者产生白色沉淀 | |
| D. | 实验室利用锌片和稀硫酸制H2时,为了加快制H2的反应速率可加入Cu(NO3)2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 23g乙醇含有碳氢键数为3NA | |
| B. | 标准状况下,2.24L SO3含有的分子数为0.1NA | |
| C. | 1mol 过氧化氢完全分解,电子转移数为1NA | |
| D. | 常温下,1L 0.5mol/L的FeCl3溶液中,所含Fe3+数为0.5NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu、Fe、Ag | B. | Cl、Br、I | C. | Na、Cu、Hg | D. | F、Br、I |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油的分馏和煤的液化都是发生了物理变化 | |
| B. | 乙烯和乙炔都能与溴水发生加成反应且生成的产物相同 | |
| C. | 甲烷和氯气反应生成一氯甲烷与苯和硝酸反应生成硝基苯的反应类型相同 | |
| D. | 苯能使酸性高锰酸钾溶液褪色,也能使溴的四氯化碳溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
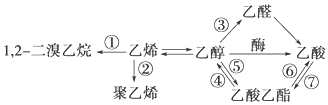
| A. | 反应①是加成反应 | B. | 只有反应②是加聚反应 | ||
| C. | 只有反应⑦是取代反应 | D. | 反应③是氧化反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com