
| A. | 氢氧化钠与盐酸; 氢氧化钠与碳酸 | |
| B. | BaCl2溶液与Na2SO4溶液; Ba(OH)2溶液与H2SO4溶液 | |
| C. | Na2CO3溶液与硝酸溶液; CaCO3溶液与硝酸溶液 | |
| D. | 石灰石与硝酸反应; 石灰石与盐酸 |
分析 A.盐酸为强酸,而碳酸为弱酸;
B.BaCl2溶液与Na2SO4溶液生成硫酸钡沉淀和氯化钠,Ba(OH)2溶液与H2SO4溶液生成硫酸钡和水;
C.碳酸钠为易溶性盐,碳酸钙为沉淀;
D.二者反应实质都是碳酸钙与氢离子反应生成钙离子和水、二氧化碳.
解答 解:A.盐酸为强酸,书写离子方程式应拆开,而碳酸为弱酸,应保留化学式,所以二者的离子反应不同,故A不选;
B.BaCl2溶液与Na2SO4溶液反应的离子反应为Ba2++SO42-═SO4↓,但Ba(OH)2溶液与H2SO4溶液除生成硫酸钡沉淀还生成水,则二者离子反应不同,故B不选;
C.碳酸钠为易溶性盐,书写离子方程式应拆开,碳酸钙为沉淀,应保留化学式,所以二者的离子反应不同,故C不选;
D.二者反应实质都是碳酸钙与氢离子反应生成钙离子和水、二氧化碳,都可以用离子方程式:CaCO3+2H+═Ca2++H2O+CO2↑表示,故D选;
故选:D.
点评 本题考查离子反应方程式,明确发生的离子反应是解答本题的关键,并熟悉离子反应方程式的书写方法来解答,难度不大.


 名校提分一卷通系列答案
名校提分一卷通系列答案 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案科目:高中化学 来源: 题型:选择题
| A. | 2.7 mol/L | B. | 1.35 mol/L | C. | 0.9 mol/L | D. | 0.45 mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
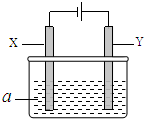 电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.
电解原理在化学工业中有广泛应用.如图表示一个电解池,其中a为电解质溶液,X、Y是两块电极板,通过导线与直流电源相连.| 方案 | X | Y | a溶液 |
| A | 银 | 石墨 | AgNO3 |
| B | 银 | 铁 | AgNO3 |
| C | 铁 | 银 | AgNO3 |
| D | 铁 | 银 | Fe(NO3)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
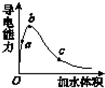 在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示,回答下列问题.
在一定温度下,向冰醋酸中加水稀释,溶液导电能力变化情况如图所示,回答下列问题.查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L | B. | 0.5L | C. | 0.3L | D. | 0.6L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com