
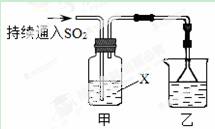
 某化学兴趣小组用以下装置探究SO2的某些化学性质。
某化学兴趣小组用以下装置探究SO2的某些化学性质。
(1)装置乙的作用是 。
(2)若X为品红溶液,观察到溶液褪色,说明SO2具有 (填序号,下同);若X为Na2S溶液,观察到溶液中出现淡黄色浑浊,说明SO2具有 。
a.氧化性 b.还原性 c.漂白性
(3)若试剂X为Ca(ClO)2溶液,可观察到白色沉淀生成,完成该过程的离子方程式:
 Ca2++
Ca2++ ClO-+
ClO-+ SO2+
SO2+ H2O=
H2O= ↓+
↓+ Cl-+
Cl-+ SO42-+
SO42-+ 。
。
科目:高中化学 来源: 题型:
用NA表示阿伏加德罗常数的值,下列叙述正确的是[ ]
A.2.24 LH2含有的原子数为0.2NA
B.常温常压下,18 g NH4+的电子数为10 NA
C.标准状况下,1 NAH2O分子占有的体积约为22.4 L
D.0.5 mol /L的AlCl3溶液中,Cl- 的数目为1.5 NA
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中含有的氯化镁是镁的重要来源之一。从海水中提取镁,可按如下步骤进行:①把贝壳制成石灰乳 ②在引入的海水中加入石灰乳,沉降、过滤,洗涤沉淀物 ③将沉淀物与盐酸反应,结晶过滤,干燥产物 ④将得到的产物熔融后电解。关于提取镁,下列说法不正确的是( )
A.此法的优点之一是原料来源丰富
B.进行①②③步骤的目的是从海水中提取MgCl2
C.以上提取镁的过程中涉及的反应都是非氧化还原反应
D.以上提取镁的过程中涉及的反应有分解反应、化合反应和复分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
有些科学家提出硅是“21世纪的能源”,这主要是由于作为半导体材料的硅在太阳能发电过程中具有重要的作用。下列有关硅的说法中,不正确的是
A. 高纯度的硅广泛用于制作计算机
B. 硅可由二氧化硅还原制得
C. 低温时,硅与水、空气和酸不反应,但能与氢氟酸反应
D. 自然界中硅的储量丰富,自然界中存在大量的单质硅
查看答案和解析>>
科目:高中化学 来源: 题型:
下列表示对应化学反应的离子方程式正确的是
A. 电解饱和NaCl溶液:2Cl-+2H+ H2↑+Cl2↑
B.向Na2SO3溶液中滴加足量NaClO溶液:SO+ ClO-= SO+ Cl-
C.向FeBr2溶液中通入足量Cl2:2Fe2++Cl2=2Fe3++2Cl-
D.向Ca(OH)2溶液中加少量NaHCO3溶液:
2 HCO+Ca2++2OH-=CaCO3↓+ CO+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法不正确的是( )
A.化学变化过程是原子的重新组合过程
B.根据化学反应中的能量变化情况,化学反应可分为吸热反应和放热反应
C.化学反应中的能量变化多少与其反应物用量有关
D.化学反应中的能量变化都是以热能形式表现出来的
查看答案和解析>>
科目:高中化学 来源: 题型:
用CH4催化还原NOx可以消除氮氧化物的污染。已知CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1。若在标准状况下4.48 L CH4恰好能将一定量NO2还原成N2和H2O(g),则整个过程中放出的热量为( )
A.114.8 kJ B.232 kJ
C.368.8 kJ D.173.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
氧化还原反应广泛应用于金属的冶炼。下列说法不正确的是( )
A.电解熔融氯化钠制取金属钠的反应中,钠离子被还原,氯离子被氧化
B.湿法炼铜与火法炼铜的反应中,铜元素都发生还原反应
C.用磁铁矿炼铁的反应中,1 mol Fe3O4被CO还原成Fe,转移9 mol e-
D.铝热法还原铁的反应中,放出的热量能使铁熔化
查看答案和解析>>
科目:高中化学 来源: 题型:
将a g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得参加反应的HCl为0.08 mol,放出标准状况下气体0.224 L.则下列判断中正确的是
A.原混合物中n(Fe)∶n(Fe2O3)=2∶1
B.向溶液中滴入KSCN溶液,显红色
C.无法计算原混合物的质量a
D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com