
【题目】萜品醇可作为消毒剂、抗氧化剂、溶剂和医药中间体。合成α-萜品醇(G)的路线之一如下:
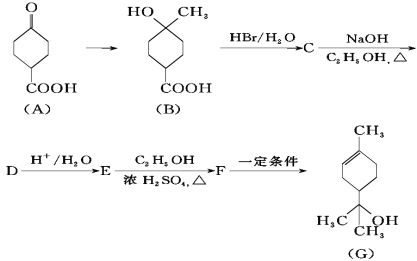
其中E的化学式为C8H12O2,请回答下列问题:
(1)A中含有的官能团名称是_____,C的结构简式为_____;
(2)由化合物C制取化合物D的反应类型为_____;
(3)试写出由化合物E制取化合物F的化学方程式:_____;
(4)化合物A满足下列条件的同分异构体有____种。
a.为链状有机物且无支链
b.能发生银镜反应
c.能和碳酸氢钠反应生成气体
(5)下列说法正确的是____(填写序号)。
a.A的核磁共振氢谱有4种峰
b.B可与FeCl3溶液发生显色反应
c.G中所有原子可能在同一平面上
d.G可以使溴水褪色
【答案】羰基、羧基  消去反应
消去反应 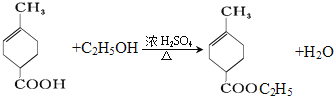 4 ad
4 ad
【解析】
依据已知物质的结构简式和反应条件,可得出C为 ,D的结构简式为
,D的结构简式为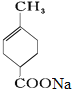 ,E的结构简式为
,E的结构简式为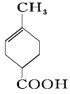 F的结构简式为
F的结构简式为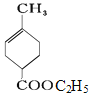 。
。
(1)由A的结构简式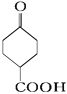 ,可得出含有的官能团名称为羰基、羧基,如上分析,得出C的结构简式为
,可得出含有的官能团名称为羰基、羧基,如上分析,得出C的结构简式为 。答案为:羰基、羧基;
。答案为:羰基、羧基; ;
;
(2)由化合物C制取化合物D的反应条件为NaOH的醇溶液,可推知反应类型为消去反应。答案为:消去反应;
(3)由化合物E制取化合物F的化学方程式 。
。
(4)化合物A满足的下列条件:a.为链状有机物且无支链,表明没有取代基;b.能发生银镜反应,含有-CHO;c.能和碳酸氢钠反应生成气体,含有-COOH;由此得出化合物A满足条件的同分异构体为OHCCH=CHCH2CH2CH2COOH、OHCCH2CH=CHCH2CH2COOH、OHCCH2CH2CH=CHCH2COOH、OHCCH2CH2CH2CH=CHCOOH,共4种。答案为:4;
(5)a.A的核磁共振氢谱有4种峰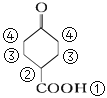 ,a正确;
,a正确;
b. 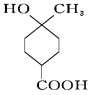 没有酚羟基,不能与FeCl3溶液发生显色反应,b错误;
没有酚羟基,不能与FeCl3溶液发生显色反应,b错误;
c.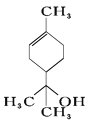 中含有多个饱和碳原子,根据甲烷的结构可知分子中所有原子不可能在同一平面上,c错误;
中含有多个饱和碳原子,根据甲烷的结构可知分子中所有原子不可能在同一平面上,c错误;
d.  含有碳碳双键,可以使溴水褪色,d正确。
含有碳碳双键,可以使溴水褪色,d正确。
故选ad。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】已知2SO2(g)+O2(g) ![]() 2SO3(g),起始时SO2和O2分别为20 mol和10 mol,达到平衡时SO2的转化率为80%。若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为( )
2SO3(g),起始时SO2和O2分别为20 mol和10 mol,达到平衡时SO2的转化率为80%。若从SO3开始进行反应,在相同的条件下,欲使平衡时各成分的体积分数与前者相同,则起始时SO3的物质的量及SO3的转化率分别为( )
A.10 mol 10% B.20 mol 20% C.20 mol 40% D.30 mol 80%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课题组以苯为主要原料,采取以下路线合成利胆药——柳胺酚。
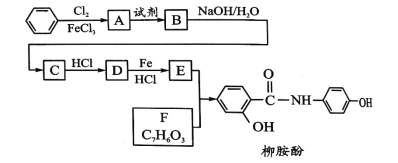
已知:
(1)对于柳胺酚,下列说法正确的是_____;
A.1mol柳胺酚最多可以和7molH2加成
B.不发生硝化反应
C.可发生消去反应
D.可与溴发生取代反应
(2)写出A→B反应所需的试剂_____;
(3)写出B→C的化学方程式______;
(4)写出化合物F的结构简式____;
(5)写出化合物E中官能团的的结构简式_____;
(6)写出同时符合下列条件的F的同分异构体的结构简式_____(写出3种)。
①属酚类化合物,且苯环上有三种不同化学环境的氢原子;②能发生银镜反应(有醛基)
(7)以苯为原料合成苯胺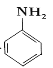 ,请设计合成路线(无机试剂及溶剂任选)_____。注:合成路线的书写格式参照如下示例流程图:CH3CHO
,请设计合成路线(无机试剂及溶剂任选)_____。注:合成路线的书写格式参照如下示例流程图:CH3CHO![]() CH3COOH
CH3COOH![]() CH3COOCH2CH3。
CH3COOCH2CH3。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,将浓度均为0.1 mol·L-1,体积分别为Va和Vb的HA溶液与BOH溶液按不同体积比混合,保持Va+Vb=100 mL,Va、Vb与混合液pH的关系如图所示,下列说法正确的是
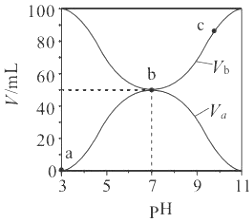
A. Ka(HA)=1×10-6
B. b点c(B+)=c(A-)=c(OH-)=c(H+)
C. a→c过程中水的电离程度始终增大
D. c点时,c(A-)/[c(OH-)c(HA)]随温度升高而减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,在2L密闭容器中,A、B、C三种气体的物质的量随时间变化曲线如图所示(其中C为有色气体),按要求解决下列问题。
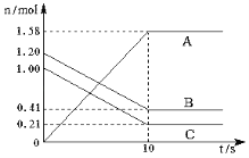
(1)该反应的化学方程式为____;
(2)用B表示的反应速率为____;
(3)下列条件改变时,能加快化学反应速率的是__请填代号)
A.扩大容器的容积 B.增大C的用量 C.降低体系的温度 D.加入催化剂
(4)该反应达到平衡状态的标志是________;
①2 v (A)=v (B) ②单位时间内生成n mol B的同时生成2n mol A ③A、B、C的浓度之比为2:1:1 ④混合气体的颜色不再改变 ⑤混合气体的密度不再改变的状态 ⑥混合气体的平均相对分子质量不再改变.
(5)该反应达到化学反应限度时,B的转化率为__。(请保留一位小数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜是重要的金属,广泛应用于电气、机械制造、国防等领域,铜的化合物在科学研究和工农业生产中有许多用途。回答下列问题:
(1)CuSO4晶体中S原子的杂化方式为________,SO42-的立体构型为_______________。
(2)超细铜粉可用作导电材料、催化剂等,其制备方法如下:
![]()
①NH4CuSO3中金属阳离子的核外电子排布式为__________________。N、O、S三种元素的第一电离能大小顺序为__________________________(填元素符号)。
②向CuSO4溶液中加入过量氨水,可生成[Cu(NH3)4]SO4,下列说法正确的是________
A.氨气极易溶于水,原因之一是NH3分子和H2O分子之间形成氢键的缘故
B.NH3分子和H2O分子,分子空间构型不同,氨气分子的键角小于水分子的键角
C.Cu(NH3)4]SO4溶液中加入乙醇,会析出深蓝色的晶体
D.已知3.4 g氨气在氧气中完全燃烧生成无污染的气体,并放出a kJ热量,则NH3的燃烧热的热化学方程式为:NH3(g)+3/4O2(g)=1/2N2(g)+3/2H2O(g) ΔH=-5a kJ·mol-1
(3)硫酸铜溶液中滴入氨基乙酸钠(H2NCH2COONa)即可得到配合物A,其结构如下左图所示。


①1 mol氨基乙酸钠(H2NCH2COONa)含有σ键的数目为________________。
②氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体:____________(写化学式)。
③已知:硫酸铜灼烧可以生成一种红色晶体,其结构如上右图所示。则该化合物的化学式是________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列事实,不能用勒夏特列原理解释的是
A. 用排饱和氯化钠溶液的方法来收集氯气
B. 配制和保存硫酸铁溶液常加入适量稀硫酸
C. 向氢氧化镁悬浊液中加入饱和氯化铵溶液,溶液变澄清
D. 对2 HI (g)![]() H2 (g) + I2 (g)的平衡体系,增大压强使颜色变深
H2 (g) + I2 (g)的平衡体系,增大压强使颜色变深
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某种合成药物中间体X的结构简式如图所示。下列说法正确的是

A.X分子中不存在手性碳原子
B.一定条件下,X可以发生加聚反应
C.1 mol X跟足量浓溴水反应,最多消耗1 mol Br2
D.1 mol X跟足量NaOH溶液反应,最多消耗3 mol NaOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用滴定管量取一定体积的浓氯水置于锥形瓶中,用NaOH溶液以恒定速度来滴定该浓氯水,根据测定结果绘制出ClO-、ClO3-等离子的物质的量浓度c与时间t的关系曲线如下。下列说法正确的是( )

A.NaOH溶液和浓氯水可以使用同种滴定管盛装
B.a点溶液中存在如下关系:c(Na+) + c(H+) = c(ClO-)+ c(OH-)+ c(ClO3-)
C.b点溶液中各离子浓度:c(Na+) > c(Cl-) > c(ClO-) = c(ClO3-)
D.t2~t4,ClO-的物质的量下降的原因可能是ClO-自身歧化:2ClO-= Cl-+ ClO3-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com