
 转化关系:
转化关系: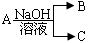 ,(若产物中有水生成则省略未表示出来)。
,(若产物中有水生成则省略未表示出来)。 ,且其在电子工业中有着重要的用途,则工业制取A化学方程式为 ;
,且其在电子工业中有着重要的用途,则工业制取A化学方程式为 ;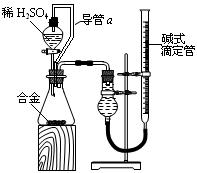
 ;
;科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
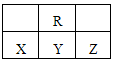
| A.R的气态氢化物比Y的气态氢化物稳定 |
| B.原子半径大小顺序是Z>Y>X |
| C.Y、R形成的化合物YR2能使KMnO4溶液褪色 |
| D.X、Y、Z中X的最高价氧化物对应的水化物的酸性最强 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
A.N2的电子式: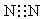 |
| B.106g的乙醇和丙醇混合液完全燃烧生成的CO2为112L(标准状况) |
C.邻羟基苯甲酸的结构简式: |
| D.131 53I质子数为53,中子数为78的碘原子: |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原子半径:A>B>D>C | B.原子序数:d>c>b>a |
| C.离子半径:C>D>B>A | D.单质的还原性:A>B>D>C |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.工业上利用热还原法冶炼金属Fe、Cr、Mn |
| B.Fe位于元素周期表的第四周期、第ⅧB族 |
C.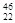 TiO2、 TiO2、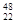 TiO2、 TiO2、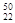 TiO2互为同位素 TiO2互为同位素 |
D.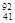 Nb3+原子核内有51个中子,核外有44个电子 Nb3+原子核内有51个中子,核外有44个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com