
 4NO2(g)£«O2(g)£»¦¤H£¾0
4NO2(g)£«O2(g)£»¦¤H£¾0| t/s | 0 | 500 | 1000 |
| c(N2O5)/mol”¤L£1 | 5.00 | 3.52 | 2.48 |
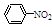 £»£Ø3·Ö£©£Ø2£©¢Ł²»±ä£Ø3·Ö£© ¢Ś0.00296 mol”¤L£1”¤s£1£Ø3·Ö£©
£»£Ø3·Ö£©£Ø2£©¢Ł²»±ä£Ø3·Ö£© ¢Ś0.00296 mol”¤L£1”¤s£1£Ø3·Ö£©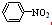 ”£
ӣ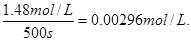



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®»Æѧ·“Ó¦ĖŁĀŹ | B£®»Æѧ·“Ó¦µÄĘ½ŗā³£Źż |
| C£®Ė®µÄĄė×Ó»ż | D£®ĪüČČ·“Ó¦·“Ó¦ĪļµÄ×Ŗ»ÆĀŹ |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ļ”ĮņĖįµÄĻ”ŹĶ | B£®µČĮæµÄŃĪĖįÓė¹żĮæµÄŠæ·Ū·“Ó¦ | C£®ĒāĘųÓėŃõĘų·“Ó¦ÖŠµÄÄÜĮæ±ä»Æ | D£®ĘųĢ¬Ēā»ÆĪļ·Šµć |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
| ĪļÖŹ n/mol T/”ę | »īŠŌĢæ | NO | E | F |
| ³õŹ¼ | 2.030 | 0.100 | 0 | 0 |
| T1 | 2.000 | 0.040 | 0.030 | 0.030 |
| T2 | 2.005 | 0.050 | 0.025 | 0.025 |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®³£ĪĀĻĀÄܹ»½ųŠŠµÄ»Æѧ·“Ó¦¶¼ŹĒ·ÅČČ·“Ó¦£¬øßĪĀĻĀ½ųŠŠµÄ·“Ó¦¶¼ŹĒĪüČČ·“Ó¦ |
| B£®³£ĪĀ³£Ń¹ĻĀ£¬pH = 1µÄŃĪĖįÖŠŌ¼ŗ¬ÓŠ6.02”Į1023øöĒāĄė×Ó |
| C£®³£ĪĀ³£Ń¹ĻĀ£¬0.5molµŖĘųŗĶĒāĘųµÄ»ģŗĻĘųĢåĢå»ż“óÓŚ11.2L |
| D£®Ōµē³Ų×°ÖƵÄÕż”¢øŗ¼«æÉŅŌŹĒĶ¬Ņ»ÖÖ½šŹō |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
 µÄŌĮĻ”£ŅŃÖŖ£ŗ
µÄŌĮĻ”£ŅŃÖŖ£ŗ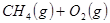
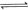



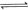
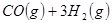


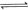


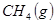 Óė
Óė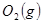 ·“Ӧɜ³É
·“Ӧɜ³É µÄČČ»Æѧ·½³ĢŹ½ĪŖ ”£
µÄČČ»Æѧ·½³ĢŹ½ĪŖ ”£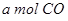 Óė
Óė £¬ŌŚ²»Ķ¬Ń¹ĒæĻĀŗĻ³É¼×“¼”£
£¬ŌŚ²»Ķ¬Ń¹ĒæĻĀŗĻ³É¼×“¼”£ µÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶Č”¢Ń¹ĒæµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£ŗ
µÄĘ½ŗā×Ŗ»ÆĀŹÓėĪĀ¶Č”¢Ń¹ĒæµÄ¹ŲĻµČēĻĀĶ¼ĖłŹ¾£ŗ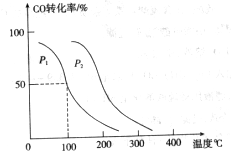

 £ØĢī”°<”±”¢”°>”±»ņ”°=”±£©
£ØĢī”°<”±”¢”°>”±»ņ”°=”±£© ”¢
”¢ Ń¹ĒæŹ±£¬Ę½ŗā³£ŹżĪŖ £ØÓĆŗ¬
Ń¹ĒæŹ±£¬Ę½ŗā³£ŹżĪŖ £ØÓĆŗ¬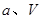 µÄ“śŹżŹ½±ķŹ¾£©”£
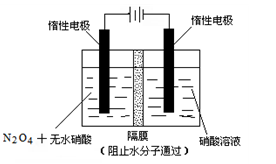
µÄ“śŹżŹ½±ķŹ¾£©”£ µē¼«ĶØČėµÄ
µē¼«ĶØČėµÄ ĪŖ £¬µē¼«·“Ó¦Ź½ŹĒ ”£
ĪŖ £¬µē¼«·“Ó¦Ź½ŹĒ ”£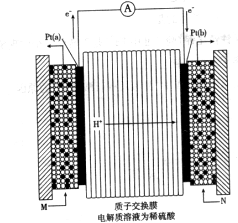
 ČÜŅŗ£¬µ±µĆµ½
ČÜŅŗ£¬µ±µĆµ½ ĶŹ±£¬²Ī¼Ó·“Ó¦µÄĘųĢå
ĶŹ±£¬²Ī¼Ó·“Ó¦µÄĘųĢå µÄĢå»żÓ¦ĪŖ
µÄĢå»żÓ¦ĪŖ  £Ø±ź×¼×“æö£©”£
£Ø±ź×¼×“æö£©”£²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĪŹ“šĢā
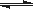 Si3N4£Øs£©+6CO£Øg£©
Si3N4£Øs£©+6CO£Øg£©| Ź±¼ä/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 | 35 | 40 | 45 |
| N2ÅضČ/mol”¤L-1 | 4£®00 | 3£®70 | 3£®50 | 3£®36 | 3£®26 | 3£®18 | 3£®10 | 3£®00 | 3£®00 | 3£®00 |
| COÅضČ/mol”¤L-1 | 0£®00 | 0£®90 | 1£®50 | 1£®92 | 2£®22 | 2£®46 | 2£®70 | | | |
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗĢīæÕĢā
|
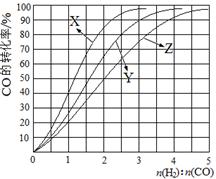
 H2(g)+CO2(g) ”÷H£¼0£¬Ä³ĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=1”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
H2(g)+CO2(g) ”÷H£¼0£¬Ä³ĪĀ¶ČĻĀøĆ·“Ó¦µÄĘ½ŗā³£ŹżK=1”£ŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ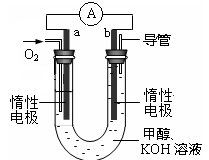
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ²»Ļź ĢāŠĶ£ŗµ„Ń”Ģā
| A£®Ļņ“æĖ®ÖŠ¼ÓČėŃĪĖįŹ¹Ė®µÄµēĄėĘ½ŗāÄęĻņŅĘ¶Æ£¬Ė®µÄĄė×Ó»ż²»±ä |
| B£®NH3(g)£«HCl(g)==NH4Cl(s)”÷H£¼0£¬µĶÓŚŅ»¶ØĪĀ¶Č×Ō·¢£¬øßÓŚŅ»¶ØĪĀ¶Č·Ē×Ō·¢ |
| C£®Ē¦Šīµē³ŲŌŚ·Åµē¹ż³ĢÖŠ£¬øŗ¼«ÖŹĮæ¼õÉŁ£¬Õż¼«ÖŹĮæŌö¼Ó |
| D£®ÓƱ„ŗĶNa2CO3ČÜŅŗ“¦ĄķBaSO4³Įµķ£¬æɽ«BaSO4×Ŗ»ÆĪŖBaCO3 |
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com