
【题目】结合元素周期表,完成下列问题。
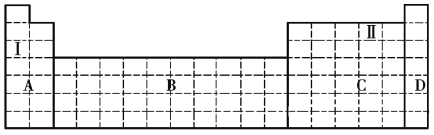
(1)在元素周期表中全部是金属元素的区域为______(填序号)。
a.A b.B c.C d.D
(2)Ⅰ和Ⅱ元素形成的化合物的化学式为______、______,它们都是____________(填“共价化合物”或“离子化合物”)。
(3)现有甲、乙两种元素,在火山口和火山附近的温泉中有甲元素的单质出现,乙元素是唯一一种原子序数比甲元素大的短周期主族元素。
①将甲、乙两元素的元素符号填写在上面元素周期表中对应的位置。______
②甲、乙两元素中,非金属性较强的是______(填元素名称),可以验证该结论的实验现象是______。
 口算小状元口算速算天天练系列答案
口算小状元口算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】如图是碳酸钙(CaCO3)在25℃和100℃两种情况下,在水中的沉淀溶解平衡曲线。下列有关说法正确的是
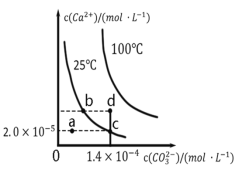
A.CaCO3(s)![]() Ca2+(aq)+CO32—(aq)ΔH<0
Ca2+(aq)+CO32—(aq)ΔH<0
B.a、b、c、d四点对应的溶度积Ksp关系:d﹥b﹥c﹥a
C.25℃时,蒸发溶剂可能使溶液由a点变为曲线上b、c之间的某一点(不含b、c)
D.25℃时CaCO3的Ksp=2.8×10-9,d点无沉淀生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CuCl晶体呈白色,熔点为430℃,沸点为1490℃,见光分解,露置于潮湿空气中易被氧化,难溶于水、稀盐酸、乙醇,易溶于浓盐酸生成H3CuCl4,反应的化学方程式为CuCl(s)+3HCl(aq)H3CuCl4(aq).
(1)实验室用如图1所示装置制取CuCl,反应原理为:
2Cu2++SO2+8Cl﹣+2H2O═2CuCl43﹣+SO![]() +4H+
+4H+
CuCl43﹣(aq)CuCl(s)+3Cl﹣(aq)

①装置C的作用是_____.
②装置B中反应结束后,取出混合物进行如图所示操作,得到CuCl晶体.
混合物![]()
![]()
![]()
![]()
![]() CuCl晶体
CuCl晶体
操作ⅱ的主要目的是_____
操作ⅳ中最好选用的试剂是_____.
③实验室保存新制CuCl晶体的方法是_____.
④欲提纯某混有铜粉的CuCl晶体,请简述实验方案:_____.
(2)某同学利用如图2所示装置,测定高炉煤气中CO、CO2、N2和O2的百分组成.
已知:
i.CuCl的盐酸溶液能吸收CO形成Cu(CO)ClH2O.
ii.保险粉(Na2S2O4)和KOH的混合溶液能吸收氧气.
①D、F洗气瓶中宜盛放的试剂分别是_____、_____.
②写出保险粉和KOH的混合溶液吸收O2的离子方程式:_____.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业合成氨反应在催化剂表面的反应历程及能量变化如图所示,下列说法正确的是

A.增大压强,①→②之间的能量差值会增大
B.合成氨的正逆反应的焓变相同
C.合成氨的过程是吸热反应
D.若使用催化剂,生成等量的NH3需要的时间更短
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于热化学反应的描述中正确的是
A.有氧气参与的反应都是放热反应
B.热化学方程式既表示能量的变化,又表示物质的变化
C.若2CO2(g)![]() 2CO(g)+O2(g)△H=+566kJ·mol-1,则CO的燃烧热△H=-566 kJ·mol-1
2CO(g)+O2(g)△H=+566kJ·mol-1,则CO的燃烧热△H=-566 kJ·mol-1
D.放热反应理论上都可以设计为原电池,将化学能转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列溶液中有关微粒的物质的量浓度关系正确的是
A.pH=8的CH3COONa溶液:c(CH3COOH)=9.9×10-7 mol·L-1
B.0.1 mol·L-1Na2SO3溶液:c(Na+)+c(H+)=c(SO32-)+c(HSO3-)+c(OH-)
C.0.1 mol·L-1NaHCO3溶液:c(Na+)+c(OH-)=c(HCO3-)+c(H2CO3)+c(H+)
D.0.1 mol·L-1CH3COONa溶液中通入HCl至溶液pH=7:c(Na+)>c(CH3COOH)>c(Cl-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度、压强下,向密闭容器中投入一定量N2和H2,发生反应:N2+3H2![]() 2NH3 △H<0。
2NH3 △H<0。
(1)反应开始阶段,v(正)_______(填“>”“<”或“=”)v(逆),随后v(正)________逐渐(填“增大”或“减小”,下同),v(逆)逐渐_______,反应达到平衡时,v(正)_______(填“>”“<”或“=”)v(逆)。
(2)达到平衡后,若正反应速率用v(N2)表示,逆反应速率用v’(H2)表示,则v(N2)=____v’(H2)。
(3)下列措施中能加快反应速率并提高氢气的转化率的是_______(填字母)。
A 其他条件不变时,压缩容器体积 B 其他条件不变时,升高反应体系温度
C 使用合适的催化剂 D 保持容器体积不变,充入一定量的氮气
(4)实际生产中往往需要将温度控制在一个合适的范围,分析温度不宜过高也不宜过低的原因是_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标况下,a克气体X与b克气体Y的分子数相同,下列说法错误的是( )
A.X和Y的式量之比是a:b
B.气体X和气体Y的密度比为b:a
C.1g气体X和1g气体Y的分子数之比是a:b
D.1mol气体X和1mol气体Y的质量比是a:b
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2016年11月30日,国际纯粹与应用化学联合会(IUPAC)公布了118号元素符号为Og,至此元素周期表的七个周期均已填满。下列关于![]() 的说法错误的是
的说法错误的是
A. 原子序数为118 B. 中子数为179
C. 核外电子数为118 D. Og的相对原子质量为297
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com