
【题目】垃圾无害化处理首先要求将垃圾分类收集。某居民小区垃圾收集点有三个垃圾桶,分别标明“厨余垃圾”、“电池”、“可回收物”。下列物质中不应投入“可回收物”桶内的是
A. 玻璃碎片 B. 破塑料盒 C. 纸制包装盒 D. 瓜皮果壳
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
【题目】下列判断哪些是正确的
①氢氧化钠是电解质
②强电解质溶液的导电性一定比弱电解质溶液导电性强
③氯化银难溶于水,所以氯化银是非电解质
④蔗糖易溶于水,所以是电解质
⑤氯气溶于水后导电,所以Cl2是电解质
A.① B.①③ C.①②⑤ D.①②③⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】医院里检测糖尿病的方法是将病人尿液加入到CuSO4和NaOH的混合液中,加热后产生红色沉淀说明病人的尿液中含有
A.脂肪 B.乙酸 C.葡萄糖 D.蛋白质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关铝及其化合物的说法错误的是( )
A.用于熔化烧碱的坩埚,可用Al2O3这种材料制成
B.铝能在空气中稳定存在是因为其表面覆盖着一层氧化铝薄膜
C.氧化铝是一种难熔物质,是一种较好的耐火材料
D.氢氧化铝能中和胃酸,可用于制胃药
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醇质子交换器膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是
①CH3OH(g)+H2O(g)→CO2(g)+3H2(g) ΔH= +49.0 kJ
②CH3OH(g)+1/2O2(g)→CO2(g)+2H2(g) ΔH=-192.9 kJ
根据上述反应,下列说法正确的是
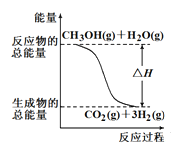
A.反应①中的能量变化如上图所示
B.可推知2H2(g)+O2(g)=2H2O(g) ΔH=-483.8KJ/mol
C.1molCH3OH充分燃烧放出的热量为192.9KJ
D.CH3OH转变成H2的过程一定要吸收热量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】各电子层排布电子的总数遵循以下规则:①每层最多容纳2n2个电子;②原子最外层电子数≤8;③原子次外层电子数≤18。决定这3条规律的电子排布规则是( )。
A. 能量最低原则
B. 泡利不相容原理
C. 洪特规则
D. 能量最低原则和泡利不相容原理
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中,正确的是( )。
A. 周期表中的主族都有非金属元素
B. 周期表中的主族都有金属元素
C. 周期表中的非金属元素都位于短周期
D. 周期表中的过渡元素都是金属元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现代传感信息技术在化学实验中有广泛的应用。某小组用传感技术测定喷泉实验中的压强变化来认识喷泉实验的原理(如图1 所示),并测定电离平衡常数Kb。

(1)实验室制取氨气的化学方程式为_____________;
图1 中用浓氨水和X 固体快速制取NH3,X固体不可以是________(填序号)
A.生石灰 B.无水氯化钙 C.烧碱 D.碱石灰
(2)关闭a,将带有装满水的胶头滴管的橡皮塞塞紧c 口,_______(填操作)可引发喷泉实验,电脑绘制三颈瓶内气压变化曲线如图2 所示。图2中________点时喷泉喷的最剧烈。
(3)喷泉实验结束后,发现水未充满三颈烧瓶(大约占体积的90 % ) ,如装置的气密性良好,烧瓶未充满水的原因是________________,所得氨水的物质的量浓度为________。
(4)从三颈瓶中用__________(填仪器名称)量取25. 00 mL氨水至锥形瓶中,用0.0500mol/LHCl 滴定测定氨水的浓度。用pH 计采集数据、电脑绘制滴定曲线如图3 所示。

当pH=11.0时,NH3·H2O电离平衡常数Kb的近似值,Kb≈_________。
(5)关于该滴定实验的说法中,正确的是_______(填序号)
A. 锥形瓶中有少量蒸馏水不影响测定结果
B.选择酚酞作为指示剂,测定结果偏高
C.酸式滴定管未用盐酸润洗会导致测定结果偏低
D.滴定终点时俯视读数会导致测定结果偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“神十搭载的长征F改进型火箭推进剂之一为无色气体N2O4,N2O4与NO2转换的热化学方程式为:N2O4(g)![]() 2NO2(g) △H=+24.4KJ/mol
2NO2(g) △H=+24.4KJ/mol
(1)将一定量N2O4投入固定容积的真空容器中,下述现象能说明反应达到平衡的是 。
a.v正(N2O4)=2v逆(NO2) b.体系颜色不变
c.气体平均相对分子质量不变 d.气体密度不变
达到平衡后,保持体积不变升高温度,再次到达平衡时,则混合气体颜色 (填“变深”、“变浅”或“不变”),判断理由 。
(2)T℃时,向1L恒容密闭容器中投入1molCH4和1molH2O(g),发生反应:CH4(g)+H2O(g)![]() CO(g)+3H2(g),经过3min,反应达到平衡。已知平衡时c(CH4)=0.5mol/L
CO(g)+3H2(g),经过3min,反应达到平衡。已知平衡时c(CH4)=0.5mol/L
①0~3min内,该反应的平均反应速率v(H2)=____________。
②T℃时,该反应的平衡常数K=___________。
(3)在一定条件下用CO和H2可以制得甲醇,CH3OH和CO的燃烧热为别725.8 kJ/mol ,283.0 kJ/mol,1 mol液态水变成气态水吸热44.0 kJ,写出甲醇不完全燃烧生成一氧化碳和气态水的热化学方程式: 。
(4)工业上用CO与H2在催化剂作用下合成CH3OH,其反应为:CO(g)+2H2(g)![]() CH3OH(g)。按n(CO) : n(H2)=1 : 2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
CH3OH(g)。按n(CO) : n(H2)=1 : 2向密闭容器中充入反应物,测得平衡时混合物中CH3OH的体积分数在不同压强下随温度的变化如图所示。
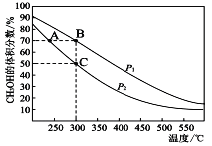
P1_________P2(填“<”“>”或“=”)
②在C点时,CO转化率为____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com