
| A. | 摩尔是把可称量物质与微观粒子联系起来的一个国际基本物理量 | |
| B. | 气体的摩尔体积与温度和压强有关,温度越高,体积越大 | |
| C. | 任何一种微观粒子,其摩尔质量以g/mol为单位,数值与这种粒子的相对分子质量或相对原子质量相同 | |
| D. | 若x个N(氮)原子的质量是1g,则阿伏加德罗常数可表示为14x mol-1 |
分析 A、物质的量是七个基本物理量之一,摩尔是物质的量的单位;
B、当温度相同时,压强越大,气体摩尔体积的数值越小;
C、以g/mol为单位时,摩尔质量在数值上等于该物质的相对分子质量或相对原子质量;
D、根据m=nM、n=$\frac{N}{{N}_{A}}$来计算.
解答 解:A、物质的量是描述微观粒子集合体的一个基本物理量,其单位为摩尔,故A错误;
B、气体摩尔体积的数值和压强、温度有关.当温度相同时,压强越大,气体摩尔体积的数值越小;当压强相同时,温度越高,气体摩尔体积的数值越大,故B错误;
C、以g/mol为单位时,摩尔质量在数值上等于该物质的相对分子质量或相对原子质量,故C正确;
D、x个N(氮)原子的物质的量n=$\frac{N}{{N}_{A}}$=$\frac{X}{{N}_{A}}$mol,其质量m=nM=$\frac{X}{{N}_{A}}$mol×14g/mol=$\frac{14X}{{N}_{A}}$g=1g,解得NA=14X/mol,故D正确.
故选CD.
点评 本题考查了阿伏伽德罗常数的有关计算,熟练掌握公式的应用和物质的结构是关键,难度不大.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
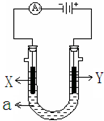 如图表示一个电解池,装有电解液a、X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解液a、X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 元素周期表中X位于Y的上一周期 | |
| B. | X的含氧酸的酸性强于Y的含氧酸的酸性 | |
| C. | 将H2X、HY分别加热至500℃,只有HY发生分解 | |
| D. | X与Y同主族,相同温度时,二者的单质与铜反应分别生成Cu2X CuY |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 向Fe(OH)2中加入足量的稀HNO3:3Fe(OH)2+10H++NO3-═3Fe3++NO↑+6H2O | |
| B. | 在强碱溶液中NaClO与Fe(OH)3反应生成Na2FeO4:3ClO+4OH-+2Fe(OH)3═3Cl-+5H2O+2FeO42- | |
| C. | 电解质溶液能够导电,是因为在通电时电解质电离产生了自由移动的离子 | |
| D. | a gC2H4和C3H6的混合物燃烧时消耗的O2一定是33.6a/14 L |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属的冶炼、电镀、燃料的燃烧、食物的腐败、钢铁的锈蚀等均属于氧化还原反应 | |
| B. | 将铁片投入硫酸铜溶液中所发生的置换反应既属于氧化还原反应,又属于离子反应 | |
| C. | 有单质参与的化学反应一定是氧化还原反应 | |
| D. | 氧化还原反应一定发生电子转移 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金的熔点高,难于融化 | |
| B. | 金的化学性质稳定,不易与其他物质反应 | |
| C. | 金越练越纯 | |
| D. | 金的硬度大,高温下难于变形 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

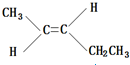 、
、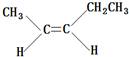 、
、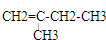 、
、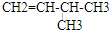 .
.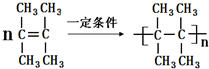 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com