
����Ŀ������������(Na2S2O5)��һ��ʳƷ���Ӽ���ʵ��������ͼ1��ʾװ���Ʊ�Na2S2O5��ʵ�鲽�����£�

������Na2CO3��Һ��ͨ��SO2��pHΪ4.1������NaHSO3��Һ��
������̼���Ʒ�ĩ����pHΪ7��8��
������ͨSO2��pHΪ4.1��
�����ӹ�������Һ������Na2S2O5���壮
(1)�Ʊ������������ܷ�Ӧ�Ļ�ѧ����ʽΪ ��
(2)Na2S2O5����ˮ����ˮ�ܷ�Ӧ��������Һ�����ԣ���ԭ���� ���������вⶨ��Һ��pH�ķ����� ��pH��4.1ʱ�����Ʒ�л��и�����仯ѧʽ�� ��
(3)���õ������ɲⶨNa2S2O5��Ʒ��+4����ĺ�����ʵ�鷽��Ϊ����һ������Na2S2O5��Ʒ�������ƿ(��ĥ��������ƿ)�У� ���ظ����ϲ���2�Σ���¼���ݣ�(ʵ���б���ʹ�õ��Լ��У�c1molL��1�ı�����Һ��c2molL��1�ı�Na2S2O3��Һ�������ᡢ������Һ������ˮ����֪��2Na2S2O3+I2�TNa2S4O6+2NaI)
(4)������ˮ�г��������۸�[Cr(��)]������Na2S2O5��FeSO47H2O�Ⱥ�������δ�����Cr2O72���ķ�ˮ��ʵ������ͼ��
��ʵ���������Һ��pH�������ߵ�ԭ���� ��
����֪��Ksp[Cr(OH)3]=6.4��10��31��lg2��0.3��c(Cr3+)��1.0��10��5molL��1ʱ��Ϊ��ȫ�������ֽ���ˮ��Cr2O72��ȫ��ת��ΪCr(OH)3����ȥ���������Һ��pH��ΧΪ ��
���𰸡�Na2CO3+2SO2�TNa2S2O5+CO2Na2S2O5��ˮ��Ӧ����NaHSO3��NaHSO3��ˮ�е���ʹ��Һ��������pH�ƣ�����ȼƣ���pH���������ⶨNa2SO3����һ������Ĺ�����c1molL��1�ı�����Һ���ټ��������ı����������ˮ����ַ�Ӧһ��ʱ�䣬���������Һ����c2molL��1��Na2S2O3��Һ�ζ�����Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ������Na2S2O5��FeSO47H2O��Cr2O72����Ӧʱ������H+��ʹ��Һ��pH���pH��5.6��
��������(1).�ɽ��������Ƶ��Ʊ����̿�֪�������Ķ��Ƿ�������ԭ��Ӧ����Ӧ����̼���ƺͶ�������������Ϊ���������ƺͶ�����̼�����������غ���ƽ��ɵã� Na2CO3+2SO2�TNa2S2O5+CO2
(2). Na2S2O5����ˮ����ˮ�ܷ�Ӧ��������Һ�����ԣ���ԭ����Na2S2O5��ˮ��Ӧ����NaHSO3��NaHSO3��ˮ������ʹ��Һ�����ԣ��������вⶨ��Һ��pH�ķ�������pH�ƣ�����ȼƣ���pH���������ⶨ��pH��4.1ʱ�����Ʒ�л��и�����仯ѧʽ��Na2SO3 ��
(3). ���õ������ɲⶨNa2S2O5��Ʒ��+4����ĺ������������ṩ���Լ��������ȼӹ����ı���Һ����������������Ϊ�����ƣ�Ϊ��ǿ��Һ�������ԣ�Ҫ���������ı�������õ�����ָʾ�����������������Һ�ζ������ĵ⣬���ݱ���Һ����������Ƶ�����������������Ƶĺ�������һ�����������+4��S�ĺ�������Ϊ�˼��ٵζ���Ҫ��������������ˮ��ʵ�鷽��Ϊ����һ������Na2S2O5��Ʒ�������ƿ�У�����һ������Ĺ�����c1molL��1�ı�����Һ���ټ��������ı����������ˮ����ַ�Ӧһ��ʱ�䣬���������Һ����c2molL��1��Na2S2O3��Һ�ζ�����Һ����ɫǡ�ñ�Ϊ��ɫ���Ұ�����ڲ���ɫ���������ظ����ϲ���2�Σ���¼���ݣ�
(4). ��ʵ������з��������ӷ�ӦΪ��3S2O32-+4Cr2O72-+26H+=6SO42-+8Cr3++13H2O��6Fe2++Cr2O72-+14H+=6Fe3++2Cr3++7H2O,������Һ��pH�������ߵ�ԭ����Na2S2O5��FeSO47H2O��Cr2O72����Ӧʱ������H+��ʹ��Һ��pH�����
���ɳ����ܽ�ƽ��Cr(OH)3![]() Cr3++3OH-��֪����Ϊc(Cr3+)��1.0��10��5molL��1ʱ��Ϊ��ȫ����,����c(OH-)>
Cr3++3OH-��֪����Ϊc(Cr3+)��1.0��10��5molL��1ʱ��Ϊ��ȫ����,����c(OH-)>![]() =
=![]() =4.0
=4.0![]() mol/L����pH>5.6�����Խ���ˮ��Cr2O72��ȫ��ת��ΪCr(OH)3����ȥ���������Һ��pH��ΧΪpH��5.6��
mol/L����pH>5.6�����Խ���ˮ��Cr2O72��ȫ��ת��ΪCr(OH)3����ȥ���������Һ��pH��ΧΪpH��5.6��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���о�NOx��SO2��CO�ȴ�����Ⱦ����Ĵ�������������Ҫ���壬��ش��������⣺
��1��һ�������£���һ���������ܱ������г���2mol SO2��1mol O2������Ӧ��������˵����ȷ���� ��
A������Ӧ����v(SO2)��v(SO3)�������˵���ÿ��淴Ӧ�Ѵﵽƽ��״̬
B�������¶Ⱥ�����������䣬����2mol N2����ѧ��Ӧ���ʼӿ�
C��ƽ��������Ӧ��Ũ�ȣ���ƽ��һ�����ƣ�����Ӧ���ת����һ��������
D��ƽ����ƶ�����ѹ�����壬ƽ��ʱSO2��O2�İٷֺ�����С��SO3�İٷֺ�������
E�������¶Ⱥ�����������䣬ƽ����ٳ���2mol SO3���ٴ�ƽ��ʱ�����Ũ�Ⱦ���ԭƽ��ʱ��Ũ�ȴ�
F��ƽ��������¶ȣ�ƽ�ⳣ��K����
��2����ij�¶��£�SO2(g)+ ![]() O2(g)
O2(g)![]() SO3(g) ��H=-98 kJ/mol����ʼʱ��100 L���ܱ������м���4.0 mol SO2(g)��10.0 mol O2(g)������Ӧ�ﵽƽ��ʱ���ų�196kJ�����������¶��µ�ƽ�ⳣ��K= ���÷�����ʾ�����ڸ��¶��£��ֱ�0.2mol/L ��SO2 ��0.1mol/L O2����̶�������ܱ������У���SO2ת����Ϊ60%ʱ���÷�Ӧ�� ���������
SO3(g) ��H=-98 kJ/mol����ʼʱ��100 L���ܱ������м���4.0 mol SO2(g)��10.0 mol O2(g)������Ӧ�ﵽƽ��ʱ���ų�196kJ�����������¶��µ�ƽ�ⳣ��K= ���÷�����ʾ�����ڸ��¶��£��ֱ�0.2mol/L ��SO2 ��0.1mol/L O2����̶�������ܱ������У���SO2ת����Ϊ60%ʱ���÷�Ӧ�� ���������
��3����һ��2L���ܱ������г���һ������SO3������Ӧ������SO3�ı仯����ͼ��ʾ����10 min��ѹ������Ϊ1L����SO3�ı仯����Ϊ ����ͼ���е���ĸ��ţ���
��4����ӦN2O4(g)![]() 2NO2(g)����H=+57kJmol-1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ� ��
2NO2(g)����H=+57kJmol-1�����¶�ΪT1��T2ʱ��ƽ����ϵ��NO2�����������ѹǿ�仯������ͼ��ʾ������˵����ȷ���ǣ� ��

A��A��C����ķ�Ӧ���ʣ�A��C
B��A��C�����������ɫ��A�Cdz
C����״̬B��״̬A�������ü��ȵķ���
D����P2��P1����ѧƽ�ⳣ��KA��KC
��5����CH4����ԭNOxҲ�������������������Ⱦ�����磺
��CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) ��H1����574KJ/mol
��CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) ��H2��-1160KJ/mol
��д��1molCH4��ԭNO2����N2��CO2��H2O��̬���ʵ��Ȼ�ѧ����ʽ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����dz��������˿���������������ijЩ�˳���֮Σ����Ϊ����ʵ�ӻ�ѧ�ĽǶ�˵�����������������������������ף���������˵�����Ǻ��˶��Ǿ��ˡ��ǣ����������Ļ�ѧԭ������ ��
A������ĵ�Ӿ B������ľ۳�
C��ѪҺ�з������ֽⷴӦ D��ѪҺ��������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijƷ�ƻ�ױƷ����Ҫ�ɷ�Z��������Ч��ԭ����������ȡ���ֿ�������ͼ��ʾ��Ӧ�ϳɡ����ж�X��Y��Z����������ȷ����

A. X��Y��Z���ܺ�NaOH��Һ��Ӧ
B. X��Z���ܺ�Na2CO3��Һ��Ӧ�������ܺ�NaHCO3��Һ��Ӧ
C. Y���ܷ����Ӿ۷�Ӧ��Ҳ�ܷ������۷�Ӧ
D. Y����������ԭ�Ӳ����ܹ�ƽ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������(H3PO2)��һ�־�ϸ������Ʒ������һԪ���ᣬ���н�ǿ�Ļ�ԭ�ԡ������й�˵����ȷ����
A. �ö��Ե缫���NaH2PO2��Һ����������ӦʽΪ��2H2O-4e-=O2��+4H+
B. H3PO2�����NaOH��Һ��Ӧ�����ӷ���ʽΪ��H3PO2+3OH-=PO23-+3H2O
C. ��H3PO2��Һ���뵽�����ظ������Һ�У�H3PO2�Ļ�ԭ�������ΪH3PO4
D. H3PO2����ˮ�ĵ��뷽��ʽΪH3PO2![]() H++ H2PO2-
H++ H2PO2-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��ͬ����Ԫ�����ʵݽ�����ʵ��ʱ���Լ������һ��ʵ�鷽��������¼���й�ʵ���������±���
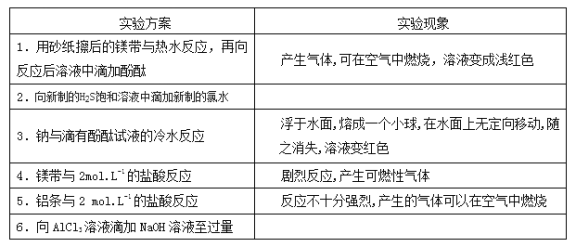
���������ͬѧ���������ʵ�鱨��
(1)ʵ��Ŀ�ģ���֤ͬ����Ԫ�ؽ����ԡ��ǽ����Եı仯���ɡ�
(2)ʵ����Ʒ���ԡ�
(3)ʵ�����ݣ�����д�����Ϣ������Ӧ��ʵ���������пո�д�����Ӧ�����ӷ���ʽ��
ʵ������ | ʵ������ | �й���������ʽ |
���� | ���� | |
�� | ______________ | ______________ |
���� | ______________ | |
�� | ���� | ���� |
�� | ���� | ______________ |
�� | ______________ | ______________ |
(4)ʵ����ۣ�______________��
(5)���������ۣ�
���ԭ�ӽṹ�����ϼ�˵�������������۵�ԭ����___________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ���������ʵ�����mgͭ���Ͻ���Ʒ��ͭ������������

����˵���в���ȷ����
A. ͭ�������������ᷴӦ���ռ�����VL����ȫΪNO
B. ����I��II��III�ֱ�Ϊ���ˡ�ϴ�ӡ�����
C. �����������VL����Ʒ����mg�ɼ���ͭ����������
D. ���õ�������ڡ�ͭ�̵��γɶ�������������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ�˼���ijFeCl2��Һ�Ƿ���ʣ���ѡ�õ��Լ��ǣ� ��
A. K3[Fe(CN)6]��Һ B. ʯ����Һ C. KSCN��Һ D. ����KMnO4��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ�м�������NaHSO4�����¶Ȳ���ʱ����Һ�� ( )
A��c(H��)/c(OH��)���� B��c(H��)��С
C��ˮ��c(H��)��c(OH��)�ij˻����� D��c(OH��)����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com