
| A. | NaHCO3═Na++H++CO32- | B. | H2SO4═2H++SO42- | ||
| C. | FeCl3═Fe3++Cl3- | D. | Ba(OH)2═Ba2++2OH- |
分析 先判断强电解质、弱电解质,强电解质在溶液中完全电离,电离方程式用等号,弱电解质在溶液中部分电离,存在电离平衡,电离方程式用可逆号,据此进行解答.
解答 解:A.NaHCO3是H2CO3的酸式盐,HCO3-不能拆,正确的电离方程式为:NaHCO3═Na++HCO3-,故①、A错误;
B.硫酸为二元强酸,在溶液中完全电离,电离方程式为:H2SO4═2H++SO42-,故B正确;
C.氯化铁为强电解质,在溶液中完全电离出铁离子和3个氯离子,正确的电离方程式为:FeCl3═Fe3++3Cl-,故C错误;
D.氢氧化钡为强电解质,其电离方程式为:Ba(OH)2═Ba2++2OH-,故D正确;
故选BD.
点评 本题考查了电离方程式的书写方法判断,掌握正确书写电离方程式的方法,并会正确判断电离方程式的正误是解题的关键,题目难度不大.


 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案科目:高中化学 来源: 题型:选择题
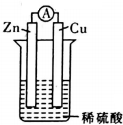 在用Zn片、Cu片和稀硫酸组成的电池装置中,下列说法中正确的是( )
在用Zn片、Cu片和稀硫酸组成的电池装置中,下列说法中正确的是( )| A. | 锌片是正极,铜片上有气泡产生 | |
| B. | 电流方向是从锌片流向铜片 | |
| C. | 溶液中的阳离子向正极移动,阴离子向负极移动 | |
| D. | 经过一段时问工作后'电解液的pH值减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
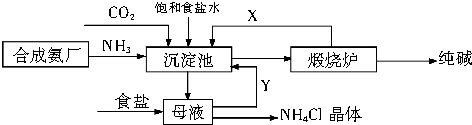
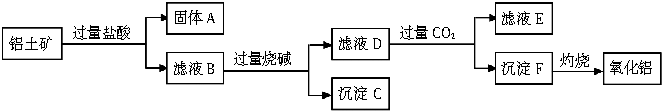
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 所含共用电子对数目为($\frac{m}{7}$+1)NA | B. | 所含碳氢键数目为$\frac{m{N}_{A}}{7}$ | ||
| C. | 燃烧时消耗的O2一定是33.6m/14 L | D. | 所含原子总数为$\frac{m{N}_{A}}{14}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 按系统命名法,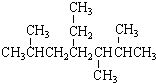 的名称为2,5,6-三甲基-4-乙基庚烷 的名称为2,5,6-三甲基-4-乙基庚烷 | |
| B. | 常压下,正戊烷、异戊烷、新戊烷的沸点依次增大 | |
| C. | 相同质量的烃,完全燃烧,消耗O2越多,烃中含ω(H)越高 | |
| D. | 乙烯和甲烷可用溴的四氯化碳溶液鉴别 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a=b | B. | a>b | C. | a<b | D. | 无法确定 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com