
【题目】下列物质的分离和鉴别方法正确的是( )
A.用分液法分离碘酒和CCl4
B.用饱和碳酸钠溶液萃取乙醇中的乙酸
C.用银氨溶液鉴别甲酸乙酯和乙醛
D.用浓溴水鉴别苯和环己烯
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的是 ( )
A. NaOH溶液通入过量CO2:OH- + CO2 = HCO3-
B. 硫化亚铁跟盐酸反应: S2- + 2H+ = H2S↑
C. Ba(OH)2与少量的NaHSO4 :Ba2++OH-+SO42- + H+=BaSO4↓+H2O
D. 电解MgCl2溶液:MgCl2 ![]() Mg + Cl2↑
Mg + Cl2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】食醋(主要成分CH3COOH )、纯碱(Na2CO3 )和小苏打(NaHCO3 )均为家庭厨房中常用的物质。已知:CH3COOH、H2CO3、HNO2的电离常数(25℃)分别为Ka=1.8×10-5;Ka1=4.3×10-7、Ka2=5.6×10-11;Ka=5.0×10-4请回答下列问题:
⑴一定温度下,向0.1mol/LCH3COOH 溶液中加入少量CH3COONa 晶体时,下列说法正确
的是_________(填代号).
a.溶液的pH增大 b.CH3COOH的电离程度增大
c.溶液的导电能力减弱 d.溶液中c(OH-)·c(H+)不变
⑵25℃时,向CH3COOH溶液中加入一定量的NaHCO3,所得混合液的pH=6,则混合液中:
c(CH3COO-)/c(CH3COOH)=______________________
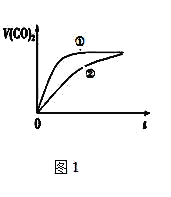
⑶常温下,将20mL 0.1 mol/L CH3COOH溶液 和20mL 0.1 mol/L HNO2 溶液分别与 20mL 0.1 mol/L NaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如图1所示,则表示CH3COOH溶液的曲线是_______(填写序号);反应结束后所得两溶液中,c(CH3COO-)________c(NO2-)(填“>”、“<”或“=”);
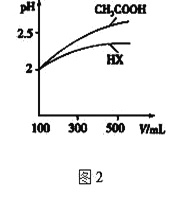
⑷体积均为100mL pH=2的CH3COOH与一元酸HX,加水稀释过程中pH与溶液体积的关系如图2所示,则HX的电离平衡常数_________(填“大于”、“小于”或“等于”)CH3COOH的电离平衡常数。
⑸25℃时,将等体积、等物质的量浓度的醋酸与氨水混合后,溶液的pH=7,则NH3·H2O的电离常数Kb =___________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】符合下列条件的有机物中,同分异构体(不考虑立体异构)数目最多的是( )
A.分子式为C5H10且能使溴的CCl4溶液褪色
B.分子式为C7H16且含有三个甲基
C.分子式为C4H8O2且能与NaOH溶液反应
D.分子式为C4H10O且能与钠反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述中正确的是( )
A、 5.6 g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA
B、常温常压下,22.4L的D2、H2组成的气体分子数约为NA
C、标准状况下,22.4LSO3中含有的氧原子数约为3 NA
D、1mol Cl2与足量NaOH溶液反应转移的电子数NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能正确表示下列反应的离子方程式的是( )
A. 钠和冷水反应 2Na+2H2O=2Na++2OH-+H2↑
B. 石灰石与醋酸溶液反应 CaCO3+2H+=Ca2++H2O+CO2↑
C. 溴化亚铁溶液中通入少量氯气 2Br -+ Cl2=Br2+2C1-
D. NH4HCO3 溶液中加入足量的 NaOH 溶液:NH4++OH-![]() NH3↑+H2O
NH3↑+H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】H2和I2在一定条件下能发生反应:H2(g)+I2(g)![]() 2HI(g)△H=-a kJmol-1。
2HI(g)△H=-a kJmol-1。
已知:

下列说法正确的是( )
A. 该反应为吸热反应
B. 断开2 mol HI分子中的化学键所需能量约为(c+b+a)kJ
C. 反应物的总能量低于生成物的总能量
D. 向密闭容器中加入2 mol H2(g)和2 mol I2(g),充分反应后放出的热量为2a kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在密闭容器中进行反应:X(g) + 3Y(g) ![]() 2Z(g),有关下列图像的说法不正确的是
2Z(g),有关下列图像的说法不正确的是
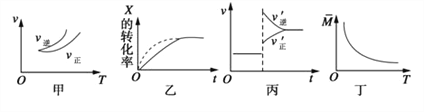
A. 依据图甲可判断正反应为放热反应
B. 在图乙中,虚线可表示使用了催化剂
C. 若正反应的ΔH<0,图丙可表示升高温度使平衡向逆反应方向移动
D. 由图丁中气体平均相对分子质量随温度的变化情况,可推知正反应的ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com