
科目:高中化学 来源: 题型:
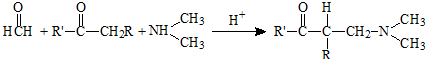
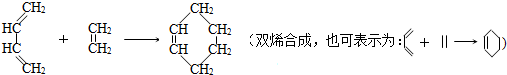
| 乙醚 | 室温 |
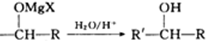 +Mg(OH)X
+Mg(OH)X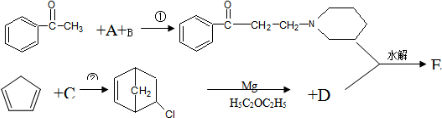
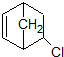 中手性碳原子数为
中手性碳原子数为查看答案和解析>>
科目:高中化学 来源: 题型:
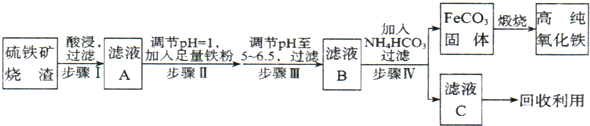
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、pH=10的NaOH和Na2CO3溶液中,水的电离程度 | B、将pH=3的盐酸和醋酸分别稀释成pH=5的溶液,需加水的体积 | C、10mL0.1 mol?L-1的醋酸与100mL 0.01 mol?L-1的醋酸中的H+物质的量 | D、物质的量浓度相等的(NH4)2SO4溶液与(NH4)2CO3溶液中NH4+的物质的量浓度 |
查看答案和解析>>
科目:高中化学 来源:2015届广东省佛山市质量检测化学试卷(解析版) 题型:填空题
(1)室温下在pH=12的NaCN溶液中,由水电离的c(OH—)为 mol•L—1。
(2)浓度为0.1mol•L—1的下列各物质的溶液中,c(NH4+)由大到小的顺序是___(填序号)。
①NH4Cl ②NH4HSO4 ③NH3•H2O ④CH3COONH4
(3)某二元酸(化学式用H2A表示)在水中的电离方程式是:
H2A=H+ +HA—,HAˉ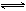 H+
+A2—。
H+
+A2—。
①则Na2A溶液显____性;NaHA溶液显 性(填“酸性”、“中性”或“碱性”)。
②若有0.1mo1•L—1Na2A的溶液,其中各种离子浓度由大到小的顺序是: (填序号)。
A.c(Na+)>c(A2—)>c(OH—)>c(HA—)>c(H+)
B.c(Na+)> c(OH—)>c(HA—)> >c(A2—) > c(H+)
C.c(Na+)> c(H+)> c(A2—)> c(OH—)>c(HA—)
D.c(A2—)>c(Na+)> c(OH—) > c(H+)>c(HA—)
(4)在含有Cl—、Br—、I—的溶液中,已知其浓度均为0.1mo1/L,已知AgCl、AgBr、AgI的溶度积分别为1.6×10—10、4.l×10—15、1.5×10—16,若向混合溶液中逐滴加入AgNO3溶液,试回答:
①当AgBr沉淀开始析出时,溶液中Ag+浓度是 。
②当AgC1沉淀开始析出时,溶液中的Br—、I—是否完全沉淀 (当溶液中离子浓度小于1.0×10—5mo1/L时,认为已经沉淀完全,本空选填“是”或“否”)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com