
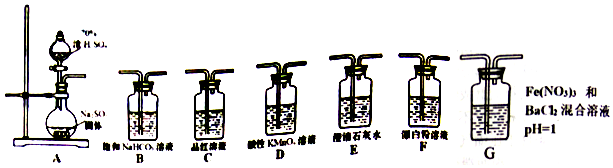
分析 (1)A中为亚硫酸钠与浓硫酸反应生成二氧化硫和硫酸钠;
(2)二氧化硫通入D中,被硝酸根氧化为硫酸根,3SO2+2NO3-+2H2O=2NO↑+3SO42-+4H+,与钡离子反应生成硫酸钡沉淀,Ba2++SO42-=3 BaSO4↓,据此分析;
(3)要验证酸性:H2SO4>H2SO3,硫酸酸性比亚硫酸酸性强,证明H2SO3>H2CO3即可,则二氧化硫应该先通入NaHCO3溶液,将生成的气体通入酸性高锰酸钾中吸收二氧化硫气体后;再将气体通入品红或者高锰酸钾或者澄清石灰水检验;
(4)要证明H2SO3的酸性强于HClO,因为二氧化硫与次氯酸根离子发生氧化还原反应,不能直接通入漂白粉溶液中,应先用二氧化硫制备二氧化碳,再通入漂白粉中,证明酸性H2SO3>H2CO3>HClO,制备的二氧化碳中有二氧化硫,故通入漂白粉之前除去二氧化硫气体,据此分析.
解答 解:(1)装置A中反应为制备二氧化硫的反应,化学方程式为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O;
故答案为:Na2SO3+H2SO4(浓)=Na2SO4+SO2↑+H2O;
(2)二氧化硫通入D中,被硝酸根氧化为硫酸根,3SO2+2NO3-+2H2O=2NO↑+3SO42-+4H+,与钡离子反应生成硫酸钡沉淀,Ba2++SO42-=3 BaSO4↓;
故答案为:①BaSO4;②3SO2+2NO3-+2H2O=2NO↑+3SO42-+4H+;
(3)二氧化硫应该先通入NaHCO3溶液,将生成的气体通入酸性高锰酸钾中吸收二氧化硫气体后,再将气体通入C品红(DKMnO4溶液),品红不褪色(D高锰酸钾),或者E澄清石灰水,澄清石灰水变浑浊,说明生成二氧化碳气体,证明H2SO3>H2CO3,又酸性:H2SO4>H2SO3,说明H2SO4的酸性强于H2CO3;
故答案为:C中品红溶液(或D中KMnO4溶液)不褪色、E中石灰水变浑浊;
(4)要证明H2SO3的酸性强于HClO,因为二氧化硫与次氯酸根离子发生氧化还原反应,不能直接通入漂白粉溶液中,证明酸性H2SO3>H2CO3>HClO即可:应先用二氧化硫制备二氧化碳,制备的二氧化碳中有二氧化硫,故通入漂白粉之前除去二氧化硫气体,再用品红检验二氧化硫是否除净,再通入漂白粉中,故顺序为:A→B→D→C→F;
故答案为:B→D→C→F.
点评 本题考查了二氧化硫的性质,涉及试剂的选择、方程式的书写、气体的检验,实验的设计等,考查知识点较多,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | CH4和Cl2光照 | B. | 氯乙烯发生加聚反应 | ||
| C. | 正丙醇、异丙醇、浓硫酸共热至170℃ | D. | 甲醇、乙醇、浓硫酸共热至140℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 100mL0.4mol/L的甲酸中含甲酸的分子数为0.04NA | |
| B. | 在标准状态下,22.4L乙烷与乙烯的混合气体,含碳原子数为2NA | |
| C. | 18g水中含有的电子数为10NA | |
| D. | NA个23Na原子的质量为23g |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验 | c(CuCl2) | 实验现象 |
| I | 0.25mol/L | 有红色固体析出,有气泡冒出,一段时间内出气速率加快. |
| II | 2.00mol/L | 反应剧烈,有红色固体析出,产生大量气泡,有白色难溶物,试管外壁温度明显升高,一段时间内出气速率加快. |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2的大量排放会导致酸雨的形成 | |
| B. | 黄河三角洲的形成体现了胶体聚沉的性质 | |
| C. | 推广使用燃料电池汽车,可减少颗粒物、CO等有害物质的排放 | |
| D. | 轮船上挂锌锭防止铁腐蚀,属于牺牲阳极的阴极保护法 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 用玻璃棒蘸取溶液X进行焰色反应实验 | 火焰呈黄色 | 溶液X中含有Na+ |
| B | 向装有Fe(NO3)2溶液的试管中加入稀H2SO4 | 在管口观察到红棕色气体 | HNO3分解成了NO2 |
| C | 在新生成的AgCl沉淀中滴入稀KI溶液,振荡 | 白色沉淀转化为黄色沉淀 | Ksp(AgCl)>Ksp(AgI) |
| D | 向饱和碳酸钠溶液中通入过量的CO2 | 溶液变浑浊 | 析出了Na2CO3 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 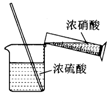 配制混酸 | B. | 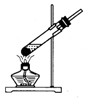 硝化反应 | C. |  分离硝基苯 | D. | 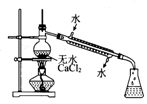 蒸馏硝基苯 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com