
 .
.
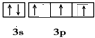
分析 (1)P原子价电子排布式为3s22p3,结合泡利原理、洪特规则画出价电子排布图;
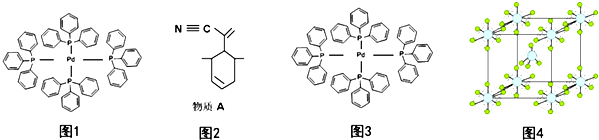
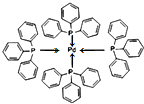
(2)P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为sp3;四(三苯基膦)钯分子为非极性分子,而水是极性分子,结合相似相溶原理判断;A分子中C原子均没有孤对电子,三键中C原子杂化轨道数目为2,双键中碳原子杂化轨道数目为3,其它碳原子杂化轨道数目为4;连接4个不同的原子或原子团的碳原子为手性碳原子;
(3)Pd含有空轨道,P原子有1对孤对电子,提供孤对电子与Pd形成配位键;
(4)PCl5是一种白色晶体,在恒容密闭容器中加热可在148℃液化,形成一种能导电的熔体,形成的正四面体形阳离子为PCl4+,正六面体形阴离子为PCl6-;
PCl3分子中P原子有一对孤电子对,PCl4+中P没有孤电子对,孤电子对对成键电子的排斥力大于成键电子对间的排斥力;
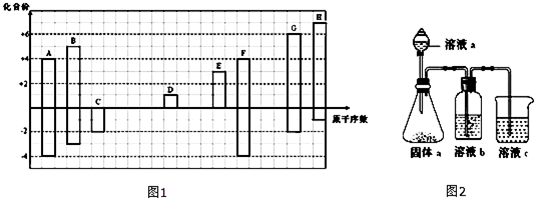
由晶胞结构可知,PCl4+位于体心,PCl6-位于顶点,由均摊法可知晶胞中含有1个PCl6-,计算晶胞质量,再根据ρ=$\frac{m}{V}$计算晶胞密度;
(5)PBr5气态分子的结构与PCl5相似,它的熔体也能导电,经测定知其中只存在一种P-Br键长,则电离生成PBr4+与Br-.
解答 解:(1)P原子价电子排布式为3s22p3,结合泡利原理、洪特规,可知价电子排布图为 ,
,
故答案为: ;
;
(2)P原子以正四面体的形态围绕在钯原子中心上,钯原子的杂化轨道类型为sp3,
水为极性分子,四(三苯基膦)钯分子为非极性分子,分子极性不相似,故不相溶,
A分子中C原子均没有孤对电子,三键中C原子杂化轨道数目为2,双键中碳原子杂化轨道数目为3,其它碳原子杂化轨道数目为4,碳原子杂化方式为:sp、sp2、sp3,
连接4个不同的原子或原子团的碳原子为手性碳原子,分子中有3个手性碳原子,
故答案为:sp3;不易溶于水,水为极性分子,四(三苯基膦)钯分子为非极性分子,分子极性不相似,故不相溶;sp、sp2、sp3;3;
(3)Pd含有空轨道,P原子有1对孤对电子,提供孤对电子与Pd形成配位键,分子中配位键为: ,
,
故答案为: ;
;
(4)PCl5是一种白色晶体,在恒容密闭容器中加热可在148℃液化,形成一种能导电的熔体,形成的正四面体形阳离子为PCl4+,正六面体形阴离子为PCl6-;
P原子杂化方式均为sp3杂化,PCl3分子中P原子有一对孤电子对,PCl4+中P没有孤电子对,孤电子对对成键电子的排斥力大于成键电子对间的排斥力,故正四面体形阳离子中键角小于PCl3的键角,
由晶胞结构可知,PCl4+位于体心,PCl6-位于顶点,由均摊法可知晶胞中含有PCl6-数目为8×$\frac{1}{8}$=1,则晶胞质量为$\frac{417}{{N}_{A}}$g,晶胞边长为a pm,则晶胞密度$\frac{417}{{N}_{A}}$g÷(a×10-10 cm)3=$\frac{4.17×1{0}^{32}}{{a}^{3}{N}_{A}}$g/cm3,
故答案为:PCl4+和PCl6-;两微粒中P原子杂化方式均为sp3杂化,PCl3分子中P原子有一对孤电子对,PCl4+中P没有孤电子对,孤电子对对成键电子的排斥力大于成键电子对间的排斥力;$\frac{4.17×1{0}^{32}}{{a}^{3}{N}_{A}}$;
(5)PBr5气态分子的结构与PCl5相似,它的熔体也能导电,经测定知其中只存在一种P-Br键长,则电离生成PBr4+与Br-,电离方程式为:PBr5=PBr4++Br-,
故答案为:PBr5=PBr4++Br-.
点评 本题是对物质结构与性质的考查,涉及核外电子排布、杂化方式、配合物、分子结构与性质、晶胞计算等,侧重考查学生对知识的迁移运用,是对学生综合能力的考查.


 小学学习好帮手系列答案
小学学习好帮手系列答案 小学同步三练核心密卷系列答案
小学同步三练核心密卷系列答案科目:高中化学 来源: 题型:选择题
| A. | ③④ | B. | ②③ | C. | ①② | D. | ②④ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
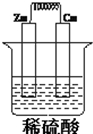 如图所示,将锌,铜通过导线相连,置于稀硫酸中构成原电池,完成下空
如图所示,将锌,铜通过导线相连,置于稀硫酸中构成原电池,完成下空查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有①⑦ | B. | 除②外都是 | C. | 只有①③ | D. | 只有①④⑥⑦ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1H、D、T属于同一种核素 | |
| B. | 含有共价键的化合物一定是共价化合物 | |
| C. | NH4Cl的电子式为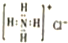 | |
| D. | S2-的结构示意图为 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 海带中提取碘的氧化过程:H2O2+2I-+2H+=I2+2H2O | |
| B. | 向NH4Al(SO4)2溶液中滴加Ba(OH)2溶液至SO42-恰好沉淀完全:Al3++2SO42-+2Ba2++4OH-=2BaSO4↓+AlO2-+2H2O | |
| C. | FeCl3溶液中通入过量的H2S气体:2Fe3++H2S=S↓+2Fe2++2H+ | |
| D. |  溶液通入少量CO2: 溶液通入少量CO2: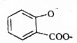 +CO2+H2O→ +CO2+H2O→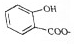 +HCO3- +HCO3- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com