
在四种化合物中①NaHCO3 ②Al(OH)3 ③(NH4)2S ④![]() 跟盐酸和NaOH溶液都能反应的是( )
跟盐酸和NaOH溶液都能反应的是( )
A.只有②④ B.只有①② C.只有①②③ D.①②③④
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
| 元素编号 | 元素特征信息 |
| A | 最高正价和最低负价的绝对值之差为2 |
| B | 最外层电子数是内层电子数的3倍 |
| C | 1molC单质能与冷水反应,在标准状况下生成11.2LH2 |
| D | 原子最外层电子数等于其周期序数 |
| E | 负二价阴离子的电子层结构与Ar原子相同 |


查看答案和解析>>
科目:高中化学 来源: 题型:
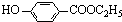 (一种常见的化妆品防霉剂),其生产过程如图(反应条件没有全部注明):
(一种常见的化妆品防霉剂),其生产过程如图(反应条件没有全部注明):




 时,不可选用的试剂是(选填编号)
时,不可选用的试剂是(选填编号)查看答案和解析>>
科目:高中化学 来源: 题型:
| 族周期 | IA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ |


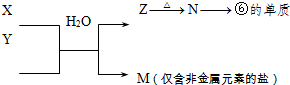
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
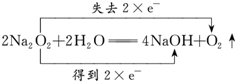
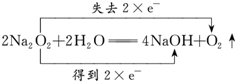
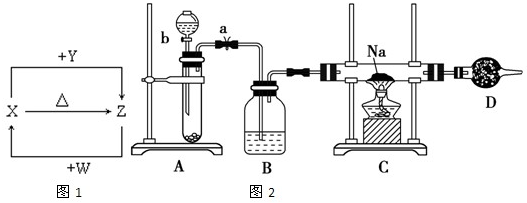
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com