
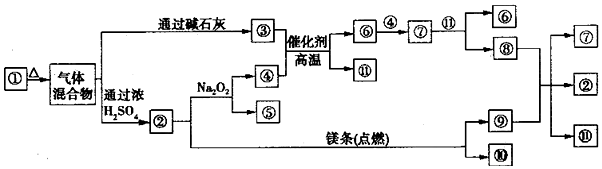

分析 突破口是②与Na2O2反应,所以②只能是CO2和H2O,因为②是通过浓硫酸的,则②只能是CO2,且产生Na2CO3和O2,④为O2,Mg与CO2反应生成MgO和C,③应为碱性气体,应为NH3,则①为NH4HCO3,阴阳离子个数比为1:1,则⑥为NO,⑦为NO2,⑧为HNO3,⑨为C;结合对应物质的性质以及题目要求可解答该题.
解答 解:(1)由以上分析可知①为NH4HCO3,②为CO2,其电子式为 ,
,
故答案为:NH4HCO3; ;
;
(2)题中涉及的氧化还原反应有③与④、④与⑤、②与⑩,⑥与④、⑦与水、⑧与⑨等反应,共6种,
故答案为:6;
(3)③与④的反应为氨气的催化氧化,化学方程式为4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O,
故答案为:4NH3+5O2$\frac{\underline{催化剂}}{△}$4NO+6H2O;
(4)⑧与⑨反应的化学方程式是C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+4NO2↑+CO2↑,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$2H2O+4NO2↑+CO2↑;
(5)④和⑦的混合气体用排水法收集,涉及反应的方程式为4NO2+O2+2H2O═4HNO3,3NO2+H2O═2HNO3+NO,
如氧气过量,设氧气为x mL,则NO2为(2a-x)mL,
根据反应方程式可得2a-(2a-x)×$\frac{5}{4}$=a,
x=$\frac{6}{5}$a,NO2为$\frac{4}{5}$a,
即二者体积为3:2,
如NO2为过量,设为NO2xmL,氧气为ymL,
则(x-5y)×$\frac{1}{3}$=a,x+y=2a,
解得x=$\frac{13}{6}$a,y=-$\frac{1}{6}$a,不符合题意,故答案为:3:2.
点评 本题考查无机物的推断,为高考常见题型,侧重于学生的分析能力、推断能力和计算能力的考查,注意把握反应的突破口,结合转化关系进行推断,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①③④⑦ | B. | ②③⑤⑦ | C. | ①④⑥⑦ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 22.4LN2中共用电子对为3NA | |
| B. | 25℃时,pH=13的Ba(OH)2溶液中含有OH-数目为0.1NA | |
| C. | 常温常压下,分子总数为NA的NO2和CO2混合气体中含有氧原子数为2NA | |
| D. | 78g苯中含有C=C键数目为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 7.1gCl2与足量NaOH溶液反应转移0.2×6.02×1023个电子 | |
| B. | 1mol羟基中含有的电子数目为9×6.02×1023个 | |
| C. | 标准状况下,2.24L辛烷含有0.8×6.02×1023个碳原子 | |
| D. | 1L 0.50mol/L Na2CO3溶液中含有1.5×6.02×1023个离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2 mol H2O的质量为36g/mol | |
| B. | NH3的摩尔质量为17g | |
| C. | 3.01×1023个SO2分子的质量为32g | |
| D. | 标准状况下,3 mol任何物质体积均为67.2L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com