
【题目】某实验小组依据反应![]() 设计如图1原电池,探究pH对AsO4 3-氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
设计如图1原电池,探究pH对AsO4 3-氧化性的影响。测得电压与pH的关系如图2。下列有关叙述不正确的是( )
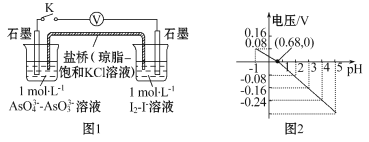
A.调节pH可以改变反应的方向 |
B.pH=0.68时,反应处于平衡状态 |
C.pH=5时, 负极电极反应式为2I--2e -= I2 |
D.pH>0.68时,氧化性I2>AsO43- |
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
【题目】根据要求完成下列实验。(a、b为弹簧夹,其他装置略去)
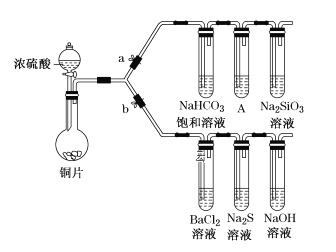
Ⅰ.验证酸性的相对强弱:碳酸>硅酸。(已知酸性:亚硫酸>碳酸)
(1)铜与浓硫酸反应的化学方程式是________________,装置A中的足量的试剂是________________。
(2)连接仪器、__________、加药品后,打开a关闭b,然后滴入浓硫酸,加热。能说明碳酸的酸性比硅酸酸性强的实验现象是__________________。
Ⅱ.验证SO2具有氧化性、还原性和酸性氧化物的通性。
(3)打开b,关闭a,能验证SO2具有氧化性的化学方程式是________________
(4)若过量的SO2通入NaOH溶液中,其化学方程式是____。
(5)BaCl2溶液中无任何现象,将其分成两份,分别滴加氨水和氯水,均产生白色沉淀,沉淀化学式是_____________________。其中SO2显示还原性并生成白色沉淀的总的离子方程式:______________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向20 mL某浓度的AlCl3溶液中滴加2 mol·L-1的NaOH溶液时,得到Al(OH)3沉淀的质量(g)与所滴加NaOH溶液的体积(mL)关系如图所示,试回答下列问题:
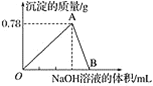
(1)图中A点表示的沉淀是__________(写化学式),其物质的量为____________。
(2)反应至A点时消耗NaOH溶液的体积为______________。
(3)图中B点溶液中的溶质有________________。
(4)AlCl3溶液的浓度为______________。
(5)O点到B点反应的总离子方程式可表示为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某柔性屏手机的柔性电池以碳纳米管做电极材料,以吸收ZnSO4溶液的有机高聚物做固态电解质,其电池总反应为:MnO2+ Zn + (1+x/6) H2O + ZnSO4![]() MnOOH + ZnSO4[Zn(OH)2]3·xH2O其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,不正确的是( )
MnOOH + ZnSO4[Zn(OH)2]3·xH2O其电池结构如图1所示,图2是有机高聚物的结构片段。下列说法中,不正确的是( )

A.碳纳米管具有导电性,可用作电极材料
B.放电时,电池的正极反应为:MnO2 + e + H+ == MnOOH
C.充电时,Zn2+移向Zn膜
D.有机高聚物是一种混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题。
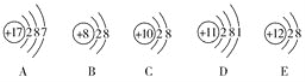
①与离子相对应的元素符号是______________,与原子相对应的离子的结构示意图是______________。
②电子层结构相同的是__________(填写代号,下同),性质最稳定的是__________,最容易失去电子的是__________,最容易得到电子的是__________。
③可直接相互结合形成的化合物的化学式是____________。可经过得失电子后再相互结合形成的化合物的化学式是______________。
④在核电荷数1~10的元素内,列举两个与B电子层结构相同的离子,写出离子的符号______________。
(2)已知元素X和Y的核电荷数均小于18,最外层电子数分别为n和(m-5),次外层有(n+2)个和m个电子,据此推断元素X和Y,其名称为X__________,Y__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D都是短周期元素,原子半径:D>C>A>B。已知A、B同周期,A、C同主族,C原子核内的质子数等于A、B原子核内的质子数之和,C原子最外层电子数是D原子最外层电子数的3倍。请回答下列问题:
(1)A元素在周期表中的位置:____;B、D两元素形成化合物的化学式:_________。
(2)元素B、C、D的简单离子半径的大小顺序:____________(用离子符号回答)。
(3)C、D两元素最高价氧化物对应水化物的碱性强弱关系: > (用化学式表示)。________
(4)B、C形成的化合物在D元素最高价氧化物对应水化物的溶液中反应的化学方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示,某同学设计了一个燃料电池并探究氯碱工业原理的相关问题,其中乙装置中X为离子交换膜。
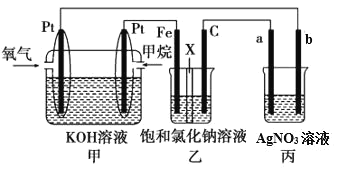
请按要求回答相关问题:
(1)甲烷燃料电池负极电极反应式是:_____。
(2)乙中X是交换膜,工作一段时间后若要恢复成原溶液,应_____。
(3)欲用丙装置给铜镀银,b应是_____(填化学式)。
(4)若乙池中的饱和氯化钠溶液换成一定量CuSO4溶液,通电一段时间后,向所得的溶液中加入0.1molCu(OH)2后恰好恢复到电解前的浓度和pH,则电解过程中转移的电子数为_____mol。(忽略溶液体积的变化)
(5)通过膜电池可除去废水中的乙酸钠和对氯苯酚(![]() ),其原理如图所示,A极的电极反应为____。
),其原理如图所示,A极的电极反应为____。

(6)化学在环境保护中起十分重要的作用,电化学降解法可用于治理水中硝酸盐污染,电化学降解NO3-的原理如图所示。
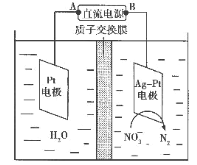
①Ag-Pt电极上的电极反应式为_____。
②若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为___g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机化合物W的分子式为C9H12 ,其含有苯环的结构有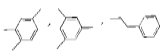 等,下列说法错误的是( )
等,下列说法错误的是( )
A. ![]() 与苯互为同系物
与苯互为同系物
B. 除了上述三种物质,W的含苯环的同分异构体还有5种
C. 有机物W的一种结构为![]() 该有机物不能与溴单质发生加成反应
该有机物不能与溴单质发生加成反应
D. 有机物W不管是否含有苯环,在一定条件下都能发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外活动小组为了探究木炭与浓硝酸反应后的气态生成物,设计如下实验。
(1)甲同学设计实验如图甲。
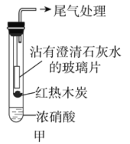
红热木炭未进入试管前,浓硝酸上方并无明显变化。当如图甲连接实验后,浓硝酸液面上方有明显的红棕色气体产生,且沾有澄清石灰水的玻璃片出现浑浊,后浑浊消失。
①液面上方出现红棕色气体,说明浓硝酸具有________(填选项字母)。
a.酸性 b.挥发性 c.不稳定性
②沾有澄清石灰水的玻璃片出现浑浊,________(填“能”或“不能”)说明木炭与浓硝酸发生了反应,是因为________。
(2)乙同学设计实验如图乙。
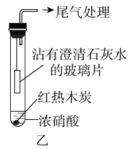
如图乙连接实验后,浓硝酸液面上方有明显的红棕色气体产生,且沾有澄清石灰水的玻璃片无明显变化。沾有澄清石灰水的玻璃片无明显变化,________(填“能”或“不能”)说明木炭与浓硝酸未反应,是因为________。
(3)丙同学克服了甲、乙同学设计上的缺点,设计实验如图丙。已知酸性高锰酸钾能将NO、NO2 氧化成 NO3-,MnO4- 被还原为 Mn2+。
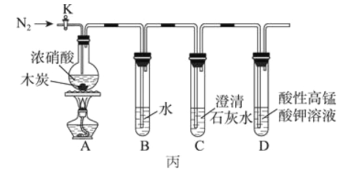
①如图连接装置后,需进行的实验操作为________;加热木炭与浓硝酸前需先通一段时间N2,目的为________________。
②装置A中木炭与浓硝酸反应的化学方程式为_________________________。
③能证明木炭被氧化的实验现象为________________________________________。
④D 装置中发生反应的离子方程式为________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com