
| A. | 电负性的大小可以作为判断金属性和非金属性强弱的尺度 | |
| B. | 在同一电子层上运动的电子,其自旋方向肯定不同 | |
| C. | 镁原子由1s22s22p63s2→1s22s22p63p2时,原子释放能量,由基态转化成激发态 | |
| D. | 原子最外层电子排布是5s1的元素,其氢氧化物一定不能溶解氢氧化铝 |
分析 A.金属的电负性一般小于1.8,非金属的电负性一般大于1.8;
B.同一电子层上运动的电子,其自旋方向有可能相同,如2p能级只容纳2个电子,自旋方向相同;
C.由能量最低原理可知基态Mg的电子排布式为1s22s22p63s2,能量处于最低状态,当变为1s22s22p63p2时,电子发生跃迁,需要吸收能量,变为激发态;
D.Rb原子最外层电子排布为5sl,RbOH为强碱,能溶解Al(OH)3.
解答 解:A.金属的电负性一般小于1.8,非金属的电负性一般大于1.8,所以电负性的大小可以作为判断金属性和非金属性强弱的尺度,故A正确;
B.同一原子轨道上运动的两个电子,自旋方向肯定不同;但同一电子层上运动的电子,其自旋方向有可能相同,如2p能级只容纳2个电子,自旋方向相同,故B错误;
C.基态Mg的电子排布式为1s22s22p63s2,由基态转化成激发态,电子能量增大,需要吸收能量,故C错误;
D.子最外层电子排布是5s1的元素,其氢氧化物可以溶解氢氧化铝,如:Rb原子最外层电子排布为5sl,RbOH为强碱,能溶解Al(OH)3,故D错误;
故选A.
点评 本题考查元素电负性含义、核外电子排布规律、原子结构与元素性质等知识,题目难度中等,明确核外电子排布规律为解答关键,注意掌握常见元素原子结构与性质的关系.


科目:高中化学 来源: 题型:选择题
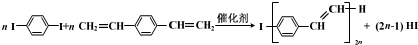
| A. | 合成PPV 的反应为加聚反应 | |
| B. | PPV 与聚苯乙烯具有相同的重复结构单元 | |
| C. | 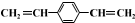 和苯乙烯互为同系物 和苯乙烯互为同系物 | |
| D. | 通过质谱法测定PPV 的平均相对分子质量,可得其聚合度 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氯碱工业的阳极反应式:2Cl--2e-═Cl2↑ | |
| B. | 钢铁吸氧腐蚀的正极反应式:O2+2H2O+4e-═4OH- | |
| C. | 碱性环境下氢氧燃料电池正极反应式:O2+2H2O+4e-═4OH- | |
| D. | 酸性环境下氢氧燃料电池负极反应式:H2-2e-+2OH-═2H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
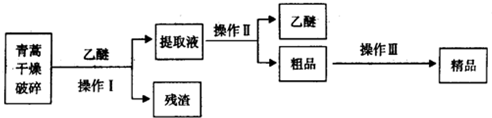
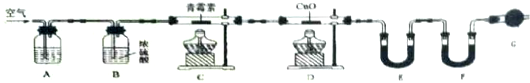
| 装置 | 实验前/g | 实验后/g |
| E | 22.6 | 42.4 |
| F | 80.2 | 146.2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 硫离子的核外电子排布式:1s22s22p6 | |
| B. | 碳原子的外围电子轨道表示式: | |
| C. | 碳-14的原子组成符号:${\;}_{6}^{14}$C | |
| D. | Cl-的结构示意图 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 并不是所有物质都含有化学键 | B. | 只有非金属原子间才能形成共价键 | ||
| C. | 单质不可能含有离子键 | D. | 共价化合物中不可能含有离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 根据下列图示变化及已知条件填空.
根据下列图示变化及已知条件填空.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
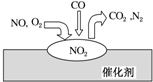 在汽车尾气净化装置里,气体在催化剂表面吸附与释放的过程如图所示.下列说法正确的是( )
在汽车尾气净化装置里,气体在催化剂表面吸附与释放的过程如图所示.下列说法正确的是( )| A. | NO是该过程的中间产物 | |
| B. | NO和O2必须在催化剂表面才能反应 | |
| C. | 汽车尾气的主要污染成分包括CO2和NO | |
| D. | 汽车尾气的主要污染物是CO和NO |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3CH2CH3 | B. | CH3CH3 | C. | CH3CH2CH2CH2CH3 | D. | CH3CH2CH2CH3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com