
【题目】NaH2PO2(次磷酸钠)易溶于水,水溶液近中性,具有强还原性,可用于化学镀银、镍、铬等。一种利用泥磷(含P4和少量CaO、Fe2O3、Al2O3、CaCl2等)为原料制备NaH2PO2·H2O的工艺流程如下:
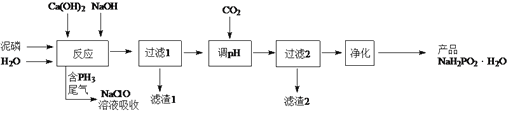
已知P4与两种碱的反应主要有:
Ⅰ. 2Ca(OH)2+P4+4H2O=2Ca(H2PO2)2+2H2↑ Ⅱ. 4NaOH + P4+8H2O = 4NaH2PO2·H2O+2H2↑
Ⅲ. 4NaOH + P4+2H2O = 2Na2HPO3 +2PH3↑ Ⅳ. NaH2PO2+NaOH = Na2HPO3+H2↑
(1) 已知H3PO2是一元中强酸,NaH2PO2是___________(填“正盐”或“酸式盐”)。
(2)尾气中的PH3被NaClO溶液吸收可生成NaH2PO2,从吸收液中获得NaH2PO2·H2O的操作为______________、______________过滤、洗涤和干燥。
(3) 用NiCl2、NaH2PO2溶液化学镀Ni,同时生成H3PO4和氯化物的化学方程式为:______________________。
(4) “反应”在温度和水量一定时,混合碱总物质的量与P4的物质的量之比[n(碱)/ n(磷)]与NaH2PO2产率的关系如图所示。当n(碱)/ n(磷)>2.6时,NaH2PO2的产率随n(碱)/ n(磷)的增大而降低的可能原因是______。
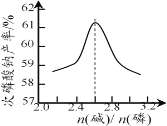
(5) 滤渣2主要成分为___________________ (填化学式)。
(6) “过滤2”的滤液须用Ag2SO4、Ba(OH) 2及Na2S溶液除去其中Cl-及Fe2+等,其中加入的Ag2SO4溶液不宜过量太多,其主要原因是_________________。
(7)在工业上,可以用惰性电极电解NaH2PO2溶液制取磷酸,请写出其阳极反应式_________________。
【答案】正盐 蒸发浓缩 冷却结晶 2NiCl2 + NaH2PO2 + 2H2O= 2Ni↓ + H3PO4 + NaCl + 3HCl 过量的碱将NaH2PO2转化为Na2HPO3 CaCO3和Al(OH)3 过量的Ag+会氧化H2PO2- H2PO2--4e-+2H2O═H3PO4+3H+
【解析】
利用泥磷(含P4和少量CaO、Fe2O3、Al2O3、CaCl2等)为原料制备NaH2PO2H2O,由流程可知,泥磷加入氢氧化钙、氢氧化钠和水,充分反应可生成PH3、氢气,PH3可用NaClO吸收,过滤,滤渣1含有磷酸钙、Fe2O3等,滤液1含有Ca(H2PO2)2、NaH2PO2以及偏铝酸钠等,通入二氧化碳调节pH,可生成氢氧化铝等、碳酸钙等,过滤,滤液主要含有NaH2PO2,经净化可得到NaH2PO2H2O,据此分析解答。
(1)H3PO2是一元中强酸,在水溶液里部分电离生成氢离子和酸根离子,电离方程式为H3PO2H++H2PO2-,H2PO2-不能再电离,则NaH2PO2为正盐,故答案为:正盐;
(2) 根据题中所给信息,PH3与NaClO反应生成NaH2PO2和NaCl,反应的离子方程式为PH3+2ClO-+OH-=H2PO2-+2Cl-+H2O,从吸收液中获得NaH2PO2·H2O,需要蒸发浓缩、冷却结晶,过滤、洗涤和干燥,故答案为:蒸发浓缩;冷却结晶;
(3)根据题意,NiCl2中Ni转化成Ni单质,NaH2PO2为还原剂,P元素的化合价升高,NiCl2+NaH2PO2→Ni↓+H3PO4+NaCl,依据化合价升降法进行配平,即2NiCl3+NaH2PO2→2Ni↓+H3PO4+NaCl,产物为H3PO4,说明该溶液为酸性,利用原子守恒配平其他物质,反应的化学方程式为2NiCl2 + NaH2PO2 + 2H2O= 2Ni↓ + H3PO4 + NaCl + 3HCl,故答案为:2NiCl2 + NaH2PO2 + 2H2O= 2Ni↓ + H3PO4 + NaCl + 3HCl;
(4)n(碱)/n(磷)>2.6,说明碱过量,根据P4与两种碱反应中IV,H2PO2-与过量的NaOH反应转化成HPO32-,次磷酸钠的产率降低,因此NaH2PO2的产率随n(碱)/n(磷)的增大而降低的可能的原因是过量的碱将NaH2PO2转化为Na2HPO3,故答案为:过量的碱将NaH2PO2转化为Na2HPO3;
(5)“调pH”除去Ca2+和Al3+,CO2与碱反应生成CO32-,CO32-与Ca2+反应生成CaCO3,CO32-与Al3+发生双水解反应生成Al(OH)3,因此滤渣2的成分是CaCO3和Al(OH)3,故答案为:CaCO3和Al(OH)3;
(6)NaH2PO2具有强还原性,Ag+具有氧化性,因此加入Ag2SO4溶液不宜过量太多,否则过量的Ag+会氧化H2PO2-,故答案为:过量的Ag+会氧化H2PO2-;
(7) NaH2PO2具有较强的还原性,电解时,阳极上H2PO2-失电子,所以用惰性电极电解NaH2PO2溶液,其阳极反应式为:H2PO2--4e-+2H2O═H3PO4+3H+,故答案为:H2PO2--4e-+2H2O═H3PO4+3H+。


 字词句段篇系列答案
字词句段篇系列答案科目:高中化学 来源: 题型:
【题目】钢铁很容易生锈而被腐蚀,每年因腐蚀而损失的钢铁占世界钢铁年产量的四分之一。请回答钢铁在腐蚀、防护过程中的有关问题。
(1)下列哪个装置可防止铁棒被腐蚀________________。

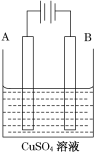
(2)在实际生产中,可在铁件的表面镀铜防止铁被腐蚀。装置示意图如图。请回答:
①A电极对应的金属是________(写元素名称),B电极的电极反应式是_________________________。
②镀层破损后,镀铜铁比镀锌铁更容易被腐蚀,请简要说明原因_________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将20g两种金属的混合物投入足量的稀硫酸中,反应完全后得到标准状况下H2 11.2L,则该混合物的组成可能是( )
A. Na和Fe B. Mg和Cu C. Al和Mg D. Zn和Fe
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
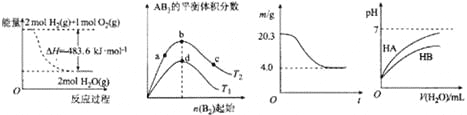
图Ⅰ 图Ⅱ 图Ⅲ 图Ⅳ
A. 图Ⅰ表示H2与O2发生反应过程中的能量变化,则H2的燃烧热△H=-241.8 kJ·mol-1
B. 图Ⅱ表示反应A2 (g)+ 3B2 (g)![]() 2AB3(g),达到平衡时A2的转化率大小为:b>a>c
2AB3(g),达到平衡时A2的转化率大小为:b>a>c
C. 图Ⅲ表示0.1mol MgCl2·6H2O在空气中充分加热时固体质量随时间的变化
D. 图Ⅳ表示常温下,稀释HA、HB两种酸的稀溶液时,溶液pH随加水量的变化,则NaA溶液的pH大于同浓度NaB溶液的pH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.1 mol·Lˉ1 NaOH溶液分别滴定体积均为20mL、浓度均为0.1 mol·Lˉ1 HCl溶液和HX溶液,溶液的pH随加入NaOH溶液体积变化如图,下列说法不正确的是( )

A. HX为弱酸
B. M点c(HX)—c(X-)﹥c(OH-)—c(H+)
C. 将P点和N点的溶液混合,呈酸性
D. 向N点的溶液中通入HCl至pH=7:c(Na+) ﹥c(HX)=c(Cl-) >c(X-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铜器久置于空气中会和空气中的水蒸气、CO2、O2作用产生“绿锈”,该“绿锈”俗称“铜绿”,又称“孔雀石”[化学式为Cu2(OH)2CO3],“铜绿”能跟酸反应生成铜盐和CO2、H2O。某同学利用下述系列反应实现了“铜![]() 铜绿
铜绿![]() ……
……![]() 铜”的转化。
铜”的转化。
铜![]() 铜绿
铜绿![]() A
A![]() Cu(OH)2
Cu(OH)2![]() B
B![]() Cu
Cu
(1)从三种不同分类标准回答,“铜绿”属于哪类物质?____。
(2)写出B的化学式____。
(3)上述转化过程中属于置换反应的是____(填序号)。
(4)写出①反应的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是一种叶绿素分子(左)和血红蛋白分子(右)的局部结构简图,下列说法不正确的是( )

A.合成叶绿素和血红蛋白分别需要镁和铁
B.植物体缺氮会影响光合作用
C.人体缺铁会影响血红蛋白对氧的运输
D.Mg和Fe分别存在于植物和动物细胞中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知存在离子反应3S+6OH-=2S2-+SO32-+3H2O,关于该反应的说法正确的是
A. 该反应属于复分解反应
B. 该反应氢氧根离子作氧化剂
C. 该反应中氧化剂与还原剂的质量为2∶1
D. 每生成2个S2-反应转移的电子数为6
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com