
已知:
①I2(g)+H2(g)  2HI(g) ΔH1=-9.48 kJ/mol
2HI(g) ΔH1=-9.48 kJ/mol
②I2(s)+H2(g)  2HI(g) ΔH2=+26.48 kJ/mol
2HI(g) ΔH2=+26.48 kJ/mol
下列判断正确的是
A.254 g I2(g)中通入2 g H2(g),反应放热9.48 kJ
B.I2(g)===I2(s) ΔH=-17.00 kJ/mol
C.固态碘的稳定性比气态碘的稳定性高
D.1 mol固态碘和1 mol气态碘分别与氢气完全反应,前者断裂的I—I键更多
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:2014高考名师推荐化学甲烷、乙烯及其同系物、苯及其同系物(解析版) 题型:选择题
现有两个热化学反应方程式:
 (l)+H2(g)
(l)+H2(g)
 (l) ΔH>0①
(l) ΔH>0①
 (l)+2H2(g)
(l)+2H2(g)
 (l) ΔH<0②
(l) ΔH<0②
下列说法中不正确的是
A.①②都属于加成反应
B.在通常条件下,①②都能自发进行
C.①吸热、②放热的事实说明苯环中含有的并不是碳碳双键
D.①②中的所有有机物均可使溴水褪色,但褪色原理不完全相同
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学物质的检验(解析版) 题型:选择题
下列有关物质检验的实验结论正确的是
| 实验操作 | 现象 | 实验结论 |
A | 向某溶液中加入盐酸酸化的氯化钡溶液 | 有白色沉淀生成 | 溶液中一定含有 |
B | 将某气体通入澄清石灰水中 | 变浑浊 | 该气体一定是CO2 |
C | 向某溶液中加入2滴KSCN溶液 | 溶液不显红色 | 溶液中一定含有Fe2+ |
另取样,先滴入氯水,再滴入KSCN溶液 | 溶液变为红色 | ||
D | 将少量某物质的溶液滴加到新制的银氨溶液中,水浴加热 | 有银镜生成 | 该物质一定是葡萄糖 |
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学燃烧热与盖斯定律(解析版) 题型:选择题
下列有关说法正确的是
A.放热反应在任何条件都能自发进行
B.应用盖斯定律,可计算某些难以直接测量的反应焓变
C.在铁制品上镀铜时,镀件为阳极,铜盐为电镀液
D.电解精炼铜时,外电路中转移电子数为2NA个时,阳极铜质量减少64g
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学燃烧热与盖斯定律(解析版) 题型:选择题
已知298K时,2SO2(g)+O2(g) 2SO3(g);△H=-197kJ·mol-1。现有同一温度下的三个体积相同的密闭容器,在第一个容器中通入2molSO2和1molO2,达到平衡时,反应放出的热量为Q1;向第二个密闭容器中通入1molSO2和0.5molO2,达到平衡时放出的热量为Q2;在第三个密闭容器中通入1molSO2、0.5molO2和1molSO3达到平衡时放出的热量为Q3。下列关系正确的是
2SO3(g);△H=-197kJ·mol-1。现有同一温度下的三个体积相同的密闭容器,在第一个容器中通入2molSO2和1molO2,达到平衡时,反应放出的热量为Q1;向第二个密闭容器中通入1molSO2和0.5molO2,达到平衡时放出的热量为Q2;在第三个密闭容器中通入1molSO2、0.5molO2和1molSO3达到平衡时放出的热量为Q3。下列关系正确的是
A.Q1=Q3=197kJ B.Q1=Q3<197kJ
C.Q1=2Q2 <197kJ D.Q2<Q1<197kJ
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学溶度积、沉淀的生成、溶解、转化(解析版) 题型:选择题
常温下,几种难溶电解质的溶度积和弱酸的电离常数如下表所示:
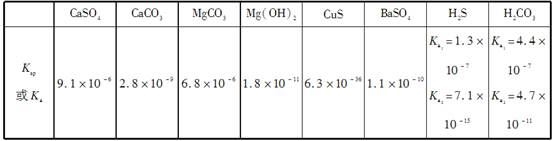
则下列说法不正确的是
A.相同温度、相同浓度的钠盐溶液的pH:Na2S>Na2CO3>NaHS>NaCl>NaHSO4
B.在NaHS溶液中滴加硫酸铜溶液,生成黑色沉淀:HS-+Cu2+=CuS↓+H+
C.除去锅炉中的水垢时,通常先加入足量硫酸钠溶液,将碳酸钙转化成硫酸钙,然后再用酸液处理
D.在Mg(HCO3)2溶液中滴加澄清石灰水发生反应的离子方程式为Mg2++2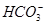 +2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O
+2Ca2++4OH-=Mg(OH)2↓+2CaCO3↓+2H2O
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学水的电离与溶液酸碱性(解析版) 题型:填空题
海底蕴藏着大量的“可燃冰”。用甲烷制水煤气(CO、H2),再合成甲醇来代替日益供应紧张的燃油。
已知:
① CH4(g)+H2O (g)=CO (g)+3H2(g) △H1=+206.2kJ·mol-1
② CH4(g)+O2(g)=CO(g)+2H2(g) △H2=-35.4 kJ·mol-1
③ CH4 (g)+2H2O (g)=CO2 (g)+4H2(g) △H3=+165.0 kJ·mol-1
(1)CH4(g)与CO2 (g)反应生成CO(g)和H2(g)的热化学方程式为 。
(2)从原料、能源利用的角度,分析反应②作为合成甲醇更适宜方法的原因是 。
(3)水煤气中的H2可用于生产NH3,在进入合成塔前常用[Cu(NH3)2]Ac溶液来吸收其中的CO,防止合成塔中的催化剂中毒,其反应是:
[Cu(NH3)2]Ac + CO + NH3  [Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)3]Ac·CO △H<0
[Cu(NH3)2]Ac溶液吸收CO的适宜生产条件应是 。
(4)将CH4设计成燃料电池,其利用率更高,装置示意如下图(A、B为多孔性石墨棒)。持续通入甲烷,在标准状况下,消耗甲烷体积VL。
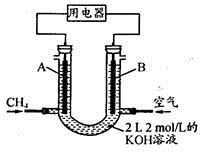
① 0<V≤44.8 L时,电池总反应方程式为 。
② 44.8 L<V≤89.6 L时,负极电极反应为 。
③ V=67.2 L时,溶液中离子浓度大小关系为 。
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氯、溴、碘及其化合物主要性质(解析版) 题型:选择题
下列叙述正确的是
A.Fe分别与氯气和稀盐酸反应所得氯化物相同
B.某无色溶液中通入Cl2,溶液变为淡黄色,再加入淀粉溶液,溶液变为蓝色,说明原溶液中存在I-
C.CO2、NO2、SO2都能与H2O反应,其反应原理相同
D.C、N、S三种单质直接与O2反应都能生成两种氧化物
查看答案和解析>>
科目:高中化学 来源:2014高考名师推荐化学氧化还原反应的概念(解析版) 题型:选择题
用高铁酸钠(Na2FeO4)对河(湖)水消毒是城市饮水处理的新技术。已知反应
Fe2O3+3Na2O2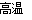 2Na2FeO4+Na2O,下列说法正确的是
2Na2FeO4+Na2O,下列说法正确的是
A.Na2O2既是氧化剂又是还原剂
B.3 mol Na2O2发生反应,有12 mol电子转移
C.在Na2FeO4中Fe为+4价,具有强氧化性,能消毒杀菌
D.Na2FeO4既是氧化产物又是还原产物
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com