
 Mn��Fe��Ϊ�������ڹ���Ԫ�أ���Ԫ�صIJ��ֵ������������ڱ���
Mn��Fe��Ϊ�������ڹ���Ԫ�أ���Ԫ�صIJ��ֵ������������ڱ���| Ԫ �� | Mn | Fe | |
| ������ /kJ•mol-1 | I1 | 717 | 759 |
| I2 | 1509 | 1561 | |
| I3 | 3248 | 2957 | |
���� ��1��ԭ�ӹ�����ڰ�����ȫ����ȫ��ʱ�������Ͷ����ȶ���
��2���ٺ��пչ���ͺ��йµ��ӶԵ�ԭ��֮�����γ���λ����
��CN-��Cԭ�Ӽ۲���ӶԸ�����2���Һ���һ���µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Cԭ���ӻ����ͣ�ԭ�Ӹ�����ȡ��۵�������ȵ�����Ϊ�ȵ����壻
��3�����Ӿ����۷е�ϵͣ�
��4�����þ�̯�ּ���ÿ��������ԭ�Ӹ�����
��� �⣺��1��MnԪ��Ϊ25��Ԫ�أ���������Ų�ʽΪ[Ar]3d54s2�����Լ۲�����Ų�ʽΪ3d54s2����Mn2+ת��ΪMn3+ʱ��3d�ܼ��ɽ��ȶ���3d5�����״̬תΪ���ȶ���3d4״̬��Ҫ�������϶ࣻ��Fe2+��Fe3+ʱ��3d�ܼ��ɲ��ȶ���3d6���ȶ���3d5�����״̬����Ҫ���������Ҫ�٣�
�ʴ�Ϊ��3d54s2�� Mn2+ת��ΪMn3+ʱ��3d�ܼ��ɽ��ȶ���3d5�����״̬ת��Ϊ���ȶ���3d4״̬����Fe2+ת��ΪFe3+ʱ��3d�ܼ��ɲ��ȶ���3d6״̬ת��Ϊ���ȶ���3d5�����״̬����
��2���ٺ��пչ���ͺ��йµ��ӶԵ�ԭ��֮�����γ���λ����Feԭ�Ӻ��пչ������Feԭ���ܺͺ��йµ��ӶԵ�ԭ�����γ���λ�����ʴ�Ϊ�����й¶Ե��ӣ�
��sCN-��Cԭ�Ӽ۲���ӶԸ�����2���Һ���һ���µ��Ӷԣ����ݼ۲���ӶԻ��������ж�Cԭ���ӻ�����Ϊsp��ԭ�Ӹ�����ȡ��۵�������ȵ�����Ϊ�ȵ����壬����������к���2��ԭ�ӡ��۵�������10���뵪�����ӻ�Ϊ�ȵ����壬��������·��˹�ṹʽΪ��N��N����
�ʴ�Ϊ��sp����N��N����
��3�����Ӿ����۷е�ϵͣ����������Ϣ֪���Ȼ����۷е�ϵͣ�Ӧ���Ƿ��Ӿ��壬�ʴ�Ϊ�����Ӿ��壻
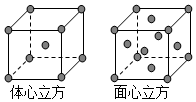
��4��������������������Feԭ�Ӹ���=8��$\frac{1}{8}$+6��$\frac{1}{2}$=4������������������Feԭ�Ӹ���=1+8��$\frac{1}{8}$=2��������������������Feԭ�Ӹ�������������������Feԭ�Ӹ���֮��=4��2=2��1���ʴ�Ϊ��2��1��
���� ���⿼�����ʽṹ�����ʣ��漰�������㡢���������жϡ�ԭ���ӻ���ʽ�жϵ�֪ʶ�㣬��ȷ���ʽṹ���۲���ӶԻ������۵�֪ʶ���ǽⱾ��ؼ���ע��·��˹�ṹʽ��ṹʽ������ʽ��������Ŀ�ѶȲ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
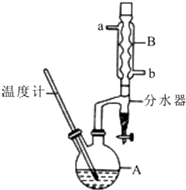 �����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�2CH3CH2CH2CH2OH$?_{135��}^{Ũ����}$��CH3CH2CH2CH2��2O+H2O����Ӧ��Ͳ����������������
�����ѳ������л���Ӧ���ܼ���ʵ�����Ʊ������ѵķ�Ӧ����Ҫʵ��װ�����£�2CH3CH2CH2CH2OH$?_{135��}^{Ũ����}$��CH3CH2CH2CH2��2O+H2O����Ӧ��Ͳ����������������| ��Է������� | �е�/�� | �ܶ�/��g/cm3�� | ˮ�е��ܽ��� | |
| ������ | 74 | 117.2 | 0.8109 | �� |
| ������ | 130 | 142.0 | 0.7704 | �������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ѹǿ | B�� | �����¶� | C�� | ����CH4Ũ�� | D�� | ������Ч���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| t/s | 0 | 500 | 1000 |
| c��N2O5����mol/L | 5.00 | 3.25 | 2.48 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����Ӧ��ϵ��ѹǿ����Ӧ�������� | |
| B�� | ����̼�ۣ�ƽ�������ƶ���ԭ����̼��O2��Ӧ���������������Ũ���ҷų����� | |
| C�� | ������ڵ�Al2O3��AlCl3���ܵõ������� | |
| D�� | �����¶ȣ���Ӧ��ƽ�ⳣ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
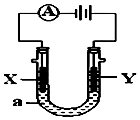 ���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺
���ԭ���ڻ�ѧ��ҵ���й㷺Ӧ�ã���ͼ��ʾһ�����أ�װ�е��Һa��X��Y������缫�壬ͨ��������ֱ����Դ��������ش��������⣺�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��H1+��H2=��H | |
| B�� | I-��H2O2�ֽⷴӦ�Ĵ��� | |
| C�� | ���ֽ�2 mol H2O2��l����������Ҫ�ṩ98 kJ������ | |
| D�� | ������1 mol O2����Ӧiiת�Ƶ��ӵ����ʵ���Ϊ2 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com