
下列事实不能用勒夏特列原理解释的是( )
A.氯水中有平衡:Cl2+H2O HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅 HCl+HClO,当加入AgNO3溶液后,溶液颜色变浅 |
B.对CO(g)+NO2(g) CO2(g)+NO(g),平衡体系增大压强可使颜色变深 CO2(g)+NO(g),平衡体系增大压强可使颜色变深 |
C.对2NO2(g)  N2O4(g), 升高温度平衡体系颜色变深 N2O4(g), 升高温度平衡体系颜色变深 |
| D.SO2催化氧化成SO3的反应,往往加入过量的空气 |
B
解析试题分析: A.氯水中有平衡:Cl2+H2O HCl+HClO,加入 AgNO3溶液后,生成AgCl沉淀,Cl―离子浓度降低,平衡向右移动,Cl2的浓度降低,溶液颜色变浅,可以用勒夏特列原理解释,A不选;B.对CO(g)+NO2(g)
HCl+HClO,加入 AgNO3溶液后,生成AgCl沉淀,Cl―离子浓度降低,平衡向右移动,Cl2的浓度降低,溶液颜色变浅,可以用勒夏特列原理解释,A不选;B.对CO(g)+NO2(g) CO2(g)+NO(g) 平衡体系增大压强,平衡不移动,二氧化氮的浓度增大,颜色变深,不能用勒夏特列原理解释,B选;C.对2NO2(g)
CO2(g)+NO(g) 平衡体系增大压强,平衡不移动,二氧化氮的浓度增大,颜色变深,不能用勒夏特列原理解释,B选;C.对2NO2(g)  N2O4(g), 是放热反应,升高温度,平衡逆向移动,平衡体系颜色变深,可以用勒夏特列原理解释,C不选;D.SO2催化氧化成SO3的反应,往往加入过量的空气,提高 O2的浓度,来提高SO2的转化率,可以用勒夏特列原理解释,D不选;选B。
N2O4(g), 是放热反应,升高温度,平衡逆向移动,平衡体系颜色变深,可以用勒夏特列原理解释,C不选;D.SO2催化氧化成SO3的反应,往往加入过量的空气,提高 O2的浓度,来提高SO2的转化率,可以用勒夏特列原理解释,D不选;选B。
考点:化学平衡移动原理


科目:高中化学 来源: 题型:单选题
下列说法正确的是( )
| A.凡是放热反应都是自发的,因为吸热反应都是非自发的 |
| B.熵增加的放热反应一定能自发进行 |
| C.自发反应一定是熵增大,非自发反应一定是熵减小或不变 |
| D.自发反应在任何条件下都能实现 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
可逆反应N2 (g)+3H2(g)  2NH3(g) △H<0,下列研究目的和示意图相符的是( )
2NH3(g) △H<0,下列研究目的和示意图相符的是( )
| | A | B | C | D |
| 研究 目的 | 压强对反应的影响 (p2>p1) | 温度对反应的影响 | 平衡体系增加N2的 浓度对反应的影响 | 催化剂对反应的影响 |
| 图 |  |  |  |  |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
已知在某密闭容器中发生反应 4NH3+5O2=4NO+6H2O,若反应速率分别用
υ(NH3)、υ(O2)、υ(NO)、υ(H2O)表示,则下列关系正确的是
A.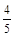 υ(NH3) =υ(O2) υ(NH3) =υ(O2) | B.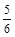 υ(O2) =υ(H2O) υ(O2) =υ(H2O) |
C.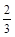 υ(NH3) =υ(H2O) υ(NH3) =υ(H2O) | D.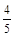 υ(O2) =υ(NO) υ(O2) =υ(NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在容积相同的五个密闭容器中分别放入等量的A2和B2,在不同温度下同时任其发生反应:A2(g)+3B2(g) 2AB3(g),分别在某一同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是
2AB3(g),分别在某一同时刻测得其中AB3所占的体积分数变化如图所示,下列说法不正确的是
| A.正反应是放热反应 | B.E、F二点尚未达到平衡 |
| C.H、I二点尚未达到平衡 | D.G、H、I三点已达平衡状态 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
可逆反应aX(g)+bY(g)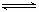 cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率( υ)一时间(t)图象如下图。则下列说法中正确的是
cZ(g)在一定温度下的一密闭容器内达到平衡后,t0时改变某一外界条件,化学反应速率( υ)一时间(t)图象如下图。则下列说法中正确的是 
| A.若a+b=c,则t0时只能是增大了容器的压强 |
| B.若a+b=c,则t0时只能是加入了催化剂 |
| C.若a+b≠c,则t0时只能是加入了催化剂 |
| D.若a+b≠c,则t0时只能是增大了容器的压强 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列是工业上制取合成氨原料气氢气的一步重要反应:CO(g)+H2O(g)  CO2(g)+H2(g) △H<0 ,该反应达到平衡后,为提高CO的转化率,下列措施中正确的是
CO2(g)+H2(g) △H<0 ,该反应达到平衡后,为提高CO的转化率,下列措施中正确的是
| A.增大压强 | B.降低温度 | C.增大CO的浓度 | D.更换催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一定温度下,向体积为2L的恒容密闭容器中充入1mol PCl5(g),发生反应:PCl5(g) PCl3(g)+Cl2(g) △H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )
PCl3(g)+Cl2(g) △H=+Q KJ/mol维持容器温度不变,测得容器内压强随反应时间的变化如图所示。下列说法正确的是( )
| A.3s内的平均速率为:V(PCl3)=0.1mol·L-1·min-1 |
| B.达到平衡时放出0.6QKJ热量 |
| C.其他条件不变,再向容器中充入1molPCl5(g),则达新平衡 时,C(PCl5)>0.4mol·L-1 |
| D.其他条件不变,增大PCl5的浓度,平衡常数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定条件下,将PCl3(g)和Cl2(g)充入体积不变的2L密闭容器中发生下述反应:
PCl3(g)+ Cl2(g)? PCl5(g);5min末达到平衡,有关数据如右表。
| | PCl3(g) | Cl2(g) | PCl5(g) |
| 初始浓度(mol?L—1) | 2.0 | 1.0 | 0 |
| 平衡浓度(mol?L—1) | C1 | C2 | 0.4 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com