
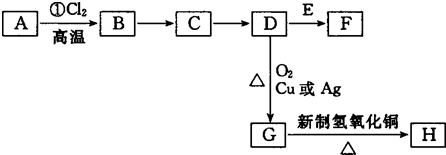
| 高温 |
| 氯气 |
| 3n |
| 2 |
| 3n |
| 2 |
 ,则高分子化合物F为
,则高分子化合物F为 ,据此解答.
,据此解答.| 3n |
| 2 |
| 3n |
| 2 |
 ,则高分子化合物F为
,则高分子化合物F为 ,
,| 水 |
| △ |
 ,D+E→F的反应方程式为:
,D+E→F的反应方程式为: ,
, ;
;| Cu |
| △ |
| Cu |
| △ |
 的同分异构体:①可以发生银镜反应,含有醛基或为甲酸形成的酯,②苯环上的一氯代物只有一种 ③遇FeCl3溶液显紫色,含有酚羟基,符合条件的同分异构体有:
的同分异构体:①可以发生银镜反应,含有醛基或为甲酸形成的酯,②苯环上的一氯代物只有一种 ③遇FeCl3溶液显紫色,含有酚羟基,符合条件的同分异构体有: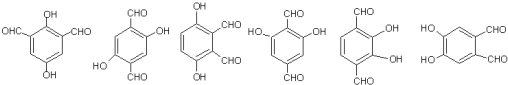 ,
, 任意2种.
任意2种.


科目:高中化学 来源: 题型:
| A、Na2CO3 |
| B、NaOH和Na2CO3 |
| C、Na2O2和Na2CO3 |
| D、Na2O2、NaOH和Na2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
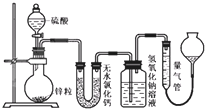 不同浓度的硫酸与锌反应时,产物不同,为了验证这一事实,某同学拟用如图装置进行实验(假设实验条件为压强为101kPa,温度为0℃).
不同浓度的硫酸与锌反应时,产物不同,为了验证这一事实,某同学拟用如图装置进行实验(假设实验条件为压强为101kPa,温度为0℃).查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
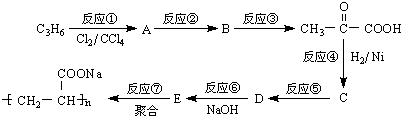
查看答案和解析>>
科目:高中化学 来源: 题型:
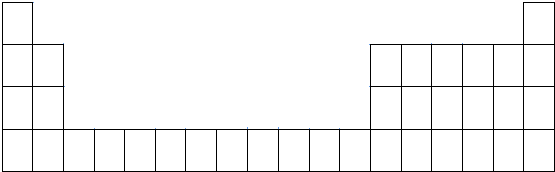
查看答案和解析>>
科目:高中化学 来源: 题型:
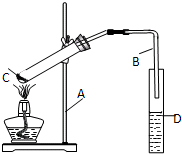 实验室制乙酸乙脂的装置如图:
实验室制乙酸乙脂的装置如图:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在蒸发皿中,用酒精灯加热蒸发NaHCO3溶液,可以得到NaHCO3固体 |
| B、用丁达尔现象可以区分食盐水和淀粉溶液 |
| C、在酸碱中和滴定实验中,锥形瓶要用待测溶液润洗 |
| D、欲配置1.0L 1.00 mol?L-1的NaCl溶液,可将58.5g NaCl溶于1.00L水中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
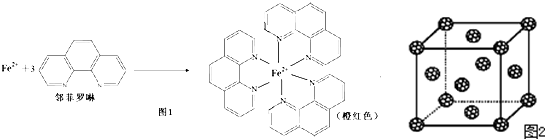
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com