
工业生产中物质的循环利用有多种模式。例如:
下列表述正确的是 ( )。
| A.图Ⅰ可用于合成氨中N2、H2的循环 |
| B.图Ⅰ可用于氨碱法制纯碱中CO2的循环 |
| C.图Ⅱ可用于电解饱和食盐水中NaCl的循环 |
| D.图Ⅲ可用于氨氧化法制硝酸中NO的循环 |
科目:高中化学 来源: 题型:填空题
磷酸盐骨水泥具有良好的生物相容性和生物活性。医药工业利用共沉淀原理,通过控制Ca/P物质的量比n(Ca)/n(P)]制备相应产品[Ca5(PO4)3OH和Ca3(PO4)2的n(Ca)/n(P)分别为1.67和15]流程如下:
(注:Ca5(PO4)3OH和Ca3(PO4)2和CaHPO4均难溶于水;Ca(H2 PO4)2溶液pH<7)
下表为n(Ca)/n(P)=1.5时,不同pH值制得滤饼的产率以及分析结果:
(1)流程中强调“滴加速度100mL/45min的作用是 。流程中调pH选氨水,不选生石灰或石灰乳的理由是 。
(2)从表中数据分析生成Ca3(PO4)2时,“pH=x”中的x的最佳取值为 ,滤饼的化学成分Ca5(PO4)3OH、Ca3(PO4)2和CaHPO4和 。
(3)酸性条件下产率偏低的原因是 。
(4)“高温煅烧”滤饼,化学反应方程式为 。
(5)如图是生产羟基磷灰石时得到的实验曲线,依据图上信息计算磷的初始浓度为0.70mmol/L,pH=10.0条件下反应前10min内磷的沉淀速率为 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
一种含铝、锂、钴的电子废料中,铝以铝箔的形式存在,钴以Co3O4的形式存在(吸附在铝箔的单面或双面),锂混杂于其中。从该废料中回收Co3O4的工艺流程如下:
(1)溶液A的溶质的主要成分为 。(填化学式)
(2)钴渣中加入稀H2SO4酸化后,再加入Na2S2O3溶液可以浸出钴离子,则浸出钴离子的离子方程式为(产物中只有一种酸根) 。
(3)在实验室模拟工业生产时,也可用盐酸浸出钴离子,但实际工业生产中不用盐酸,请从反应原理分析不用盐酸浸出钴离子的主要原因: 。
(4)加入NaF的反应为:Li++F- LiF↓,该反应的平衡常数表达式为K= 。
LiF↓,该反应的平衡常数表达式为K= 。
(5)加入30%Na2CO3溶液的作用是 。
(6)在空气中锻烧CoCO3生成Co3O4的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
K2SO4是无氯优质钾肥,Mn3O4是生产软磁铁氧体材料的主要原料。以硫酸工业的尾气联合制备K2SO4和Mn3O4的工艺流程如下:
(1)几种盐的溶解度见图。反应III中,向(NH4)2SO4溶液中加入KCl溶液充分反应后,进行蒸发浓缩、 、洗涤、干燥等操作即得K2SO4产品。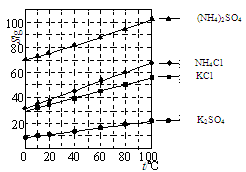
(2)检验K2SO4样品是否含有氯化物杂质的实验操作是: 。
(3)反应IV的化学方程式为 。
(4)Mn3O4与浓盐酸加热时发生反应的离子方程式为 。
(5)下图是煅烧MnSO4?H2O时温度与剩余固体质量变化曲线。
①该曲线中B段所表示物质的化学式为 。
②煅烧过程中固体锰含量随温度的升高而增大,但当温度超过1000℃时,再冷却后,测得产物的总锰含量反而减小。试分析产物总锰含量减小的原因: 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
海水占地球总储水量的97.2%,若把海水淡化和化工生产结合起来,既可解决淡水资源缺乏的问题,又可充分利用海洋资源。
(1)海水中存在大量的氯化钠,氯化钠中的金属元素位于元素周期表的________族。
(2)目前,国际上使用的“海水淡化”主要技术之一是蒸馏法。蒸馏法是将海水变成蒸气,蒸气经冷却而得高纯度的淡水。由此可判断蒸馏法是________(填“物理变化”或“化学变化”)。
(3)工业上利用电解饱和食盐水可制得重要化工产品。反应式为:
NaCl+H2O NaOH+H2↑+Cl2↑(未配平),该反应中NaCl的电子式是______;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐______t。(可能用到的相对原子质量:Na:23,Cl:35.5,H:1,O:16)
NaOH+H2↑+Cl2↑(未配平),该反应中NaCl的电子式是______;利用电解所得气体制36.5%的浓盐酸1000 t,最少需消耗食盐______t。(可能用到的相对原子质量:Na:23,Cl:35.5,H:1,O:16)
(4)近年来,有人提出了一种利用氯碱工业产品及氯化钠循环治理含二氧化硫废气并回收二氧化硫的方法。该方法流程如下图:
请写出②④的化学反应方程式:________、________。
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列关于工业生产说法错误的是( )
| A.在侯氏制碱工业中,向饱和氯化钠溶液中先通入氨气,后通入二氧化碳 |
| B.在硫酸工业、合成氨工业、硝酸工业中,皆采用循环操作提高原料利用率 |
| C.在氯碱工业,电解槽被离子交换膜隔成阴极室和阳极室 |
| D.工业上采用电解熔融氯化铝的方法制取金属铝 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
一包硫酸铵样品中,不慎混入了下列化肥:①氯化铵;②碳酸氢铵;③硝酸钾;④尿素[CO(NH2)2]中的一种。经测定,这种硫酸铵样品中含N的质量分数为23%,则混入的杂质可能是 ( )。
| A.①或② | B.①或④ |
| C.①或②或③ | D.②或③或④ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
合成NH3所需的H2可由煤与H2O反应制得,其中有一步反应为CO(g)+H2O(g) CO2(g)+H2(g) ΔH<0。欲提高CO转化率可采用的方法可能有:①降低温度;②增大压强 ③使用催化剂 ④增大CO的浓度;⑤增大水蒸气的浓度,其中正确的组合是( )。
CO2(g)+H2(g) ΔH<0。欲提高CO转化率可采用的方法可能有:①降低温度;②增大压强 ③使用催化剂 ④增大CO的浓度;⑤增大水蒸气的浓度,其中正确的组合是( )。
| A.①②③ | B.④⑤ | C.①⑤ | D.⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
下列有关合成氨工业的说法中,正确的是 ( )。
| A.从合成塔出来的混合气体中,氨气占15%,所以生产氨的工厂的效率都很低 |
| B.由于氨易液化,N2和H2在实际生产中循环使用,所以总体来说,氨的产率很高 |
| C.合成氨工业的反应温度控制在500 ℃,目的是使化学平衡向正反应方向移动 |
| D.我国合成氨厂采用的压强是10~30 MPa,因为该压强下铁触媒的活性最大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com