
下列说法中正确的是
A.三氧化硫的水溶液能导电,但是三氧化硫不是电解质
B.1 mol•L﹣1的硫酸钠溶液和1 mol•L﹣1的氢氧化钠溶液导电性相同
C.氢氧化铁胶体能导电,故氢氧化铁胶体是电解质
D.在 相同温度下,饱和溶液一定比不饱和溶液的导电性强
相同温度下,饱和溶液一定比不饱和溶液的导电性强
科目:高中化学 来源:2016-2017学年广东省高二上期中化学试卷(解析版) 题型:选择题
下列变化属于吸热反应的是 ①液态水汽化 ②将胆矾加热变为白色粉末 ③浓硫酸稀释 ④氯酸钾分解制氧气 ⑤生石灰跟水反应生成熟石灰
A、①④⑤ B、①②④ C、②③ D、②④
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上期中化学卷(解析版) 题型:选择题
已知反应:①101kPa时,2C(s)+O2(g)=2CO(g);△H=-221kJ/mol
②稀溶液中,H+(aq)+OH-(aq)=H2O(l);△H=-57.3kJ/mol 下列结论正确的是
A.碳的燃烧热等于110.5kJ/mol
B.2molC(s)在2molO2(g)燃烧, 放出221kJ热量
C.1L 0.1mol/L硫酸溶液与1L pH=11的NaOH溶液反应,放出5.73kJ热量
D.pH=3的醋酸与pH=11的NaOH溶液反应生成1mol水,放出57.3kJ热量
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上期中化学卷(解析版) 题型:选择题
常温下,在溶液中可发生以下反应:
①2Fe2++Br2═2Fe3++2Br-,②2Br-+Cl2=Br2+2Cl-,
③2Fe3++2I-═2Fe2++I2。由此判断下列说法正确的是
A.铁元素在反应①和③中均被氧化
B.反应②中当有1 mol Cl2被还原时,有2 mol Br﹣被氧化
C.氧化性强弱顺序:Cl2>Br2>I2>Fe3+
D.还原性强弱顺序:I﹣>Br﹣>Fe2+>Cl﹣
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上期中化学卷(解析版) 题型:选择题
配制250mL0.10mol•L﹣1的NaOH溶液时,下列实验操作会使配得的溶液浓度偏大是
A.转移溶液后未洗涤烧杯和玻璃棒就直接定容
B.NaOH固体溶解后立即转入容量瓶
C.在容量瓶中进行定容时仰视刻度线
D.定容后把容量瓶倒转摇匀,发现液面低于刻度,再补充几滴水至刻度
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上期中化学卷(解析版) 题型:填空题
(1)写出下列各烷烃的分子式。
①烷烃A在同温同压下,蒸气密度是H2的43倍,则A为 。
②1 L烷烃C的蒸气完全燃烧时,生成同温同压下15 L的水蒸气,则C为___________。
③烷烃D分子中含有22条共价键,则D为_____________。
(2)相对分子质量为72的烷烃,若此有机物的一氯代物分子中有两个—CH3,两个—CH2—,一个 和一个—Cl,它的可能结构有种 。
和一个—Cl,它的可能结构有种 。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上期中化学卷(解析版) 题型:选择题
高氯酸、硫酸、硝酸和盐酸都是强酸,其酸性在水溶液中差别不大。以下是某温度下这四种酸在冰醋酸中的电离常数:
酸 | HClO4 | H2SO4 | HCl | HNO3 |
Ka | 1.6×10-5 | 6.3×10-9 | 1.6×10-9 | 4.2×10-10 |
从以上表格中判断以下说法中不正确的是
A.在冰醋酸中硫酸的电离方程式为H2SO4===2H++S O
O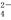
B.在冰醋酸中高氯酸是这四种酸中最强的酸
C.在冰醋酸中这四种酸都没有完全电离
D.水对于这四种 酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
酸的强弱没有区分能力,但醋酸可以区别这四种酸的强弱
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上期中化学卷(解析版) 题型:选择题
已知一种c(H+)=1×10-3 mol/L的酸溶液和一种c(OH-)=1×10-3 mol/L 的碱溶液等体积混合后,溶液呈酸性,其原因可能是
A.浓的强酸和稀的强碱溶液 B.浓的弱酸和稀的强碱溶液反应
C.等浓度的强酸和弱碱溶液反应 D.生成了一种强酸弱碱盐
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省高一上期中化学卷(解析版) 题型:选择题
将0.195 g锌粉加入到20.0 mL的0.100 mol·L-1MO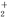 溶液中,恰好完全反应,则还原产物可能是 ( )
溶液中,恰好完全反应,则还原产物可能是 ( )
A.M2+ B.M C.M3+ D.MO2+
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com