
 ,
, .
.

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
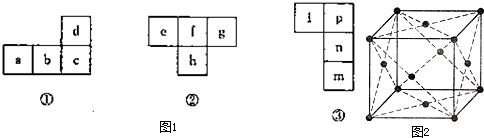
| 1 | 3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(共8分)(1) 根据杂化轨道理论,下列离子或分子:NH3、NF3、NO2+中氮分别采用 、 、 杂化轨道同相应的键合原子成键。其中NH3的键角 (填“大于”或“小于”)NF3的键角的原因是 。
(2) 最近,德国科学家在医学杂志《柳叶刀》上发表文章,他们研究发现一种名为甘草甜素的物质可以有效抑制非典病毒的增殖,有望用其研制出治疗非典的特效药。此前医学家已用甘草甜素作为有效成分开发出药物,治疗丙肝与艾滋病等,并取得了一定效果。甘草甜素(甘草素)是甘草的根和茎中所含的一种五环三萜皂苷,其结构如图1所示:

甘草甜素的(A)苷键构型为 ,将其水解可得到一分子的甘草次酸(如图2)和两分子的(填名称) ,其结构为: 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com