
【题目】 大气污染问题日益引起全民关注.
(1)PM2.5是指大气中直径小于或等于2.5μm(1μm=103nm)的颗粒物.下列说法不正确的是______(填字母序号)。
a.PM2.5主要来源于火力发电、工业生产、汽车尾气排放等过程
b.PM2.5颗粒小,所以对人体无害
c.直径介于1~2.5μm的颗粒物分散到空气中可形成胶体
d.推广使用电动汽车,可以减少PM2.5的污染
(2)某地科研工作者用五年时间研究出利用石灰乳除工业燃煤尾气中的硫(SO2、SO3)和氮(NO、NO2)的新工艺,既能净化尾气,又能获得应用广泛的CaSO4和Ca(NO2)2
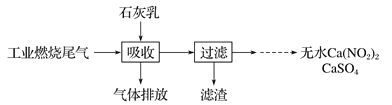
硫酸型酸雨的形成过程是大气中的SO2溶于雨水生成某种弱酸,在空气中经催化氧化生成硫酸,该过程中反应的化学方程式为___________、__________.
CaSO4可以调节水泥的硬化时间.尾气中2molSO2被石灰乳逐渐吸收最终生成了1molCaSO4,该过程中转移的电子数目为___________。
③Ca(NO2)2可制成混凝土防冻剂、钢筋阻锈剂等。尾气中NO、NO2与石灰乳反应生成Ca(NO2)2的化学方程式_________________.
(3)人类活动产生的CO2长期积累,威胁到生态环境,其减排问题受到全世界关注。
工业上常用高浓度的K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如下:
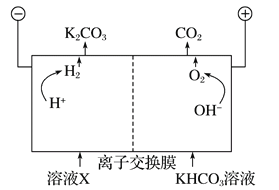
在阳极区发生的反应包括___________和H++HCO3-=H2O+CO2↑。
简述CO32-在阴极区再生的原理___________。
③再生装置中产生的CO2和H2在一定条件下反应生成甲醇,工业上利用该反应合成甲醇。
已知:25℃,101KPa下:
H2(g)+![]() O2(g)═H2O(g)△H1=-242kJ/mol
O2(g)═H2O(g)△H1=-242kJ/mol
CH3OH(g)+![]() O2(g)═CO2(g)+2H2O(g)△H2=-676kJ/mol
O2(g)═CO2(g)+2H2O(g)△H2=-676kJ/mol
写出CO2和H2生成气态甲醇等产物的热化学方程式____________.
【答案】(1)bc (2分);(2)① SO2+ H2O![]() H2SO3; 2H2SO3+ O2=2H2SO4 (每个方程式1分);② 2NA(2分) ③ NO + NO2+ Ca(OH)2= Ca(NO2)2+ H2O (2分)
H2SO3; 2H2SO3+ O2=2H2SO4 (每个方程式1分);② 2NA(2分) ③ NO + NO2+ Ca(OH)2= Ca(NO2)2+ H2O (2分)
(3)①4OH— —4e-= 2H2O + O2↑ ②答案1:HCO3–存在电离平衡:HCO3–![]() H++CO32-,阴极H+放电浓度减小平衡右移CO32-再生;答案2:阴极H+放电OH-浓度增大,OH-与HCO3–反应生成CO32-,CO32-再生 (3分) ③CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H =" -50" kJ/mol
H++CO32-,阴极H+放电浓度减小平衡右移CO32-再生;答案2:阴极H+放电OH-浓度增大,OH-与HCO3–反应生成CO32-,CO32-再生 (3分) ③CO2(g) + 3H2(g) = CH3OH(g) + H2O(g) △H =" -50" kJ/mol
【解析】试题分析:(1)a.PM2.5是指大气中直径小于或等于2.5μm的颗粒物.它的主要来源是日常发电、工业生产、汽车尾气排放等过程中经过燃烧而排放的残留物,a正确;b.PM2.5表面积大,具有吸附性,能吸附大量有毒物质,b错误;c.胶体微粒直径在10-7m~10-9m之间,PM2.5粒子的大小不符合,c错误;d.减少机动车尾气排放,减少了烟尘,能降低空气中PM2.5,d正确;答案选bc;
(2)①硫酸型酸雨形成过程是SO2溶于水生成亚硫酸,SO2+H2O![]() H2SO3;亚硫酸再被空气中的氧气氧化成硫酸,2H2SO3+O2═2H2SO4;
H2SO3;亚硫酸再被空气中的氧气氧化成硫酸,2H2SO3+O2═2H2SO4;
②尾气中SO2与氧气和石灰乳反应生成CaSO4和水,反应方程式为:2SO2+O2+2Ca(OH)2═2CaSO4+2H2O,方程式中转移4mol电子,生成1mol CaSO4转移2mol电子,个数为2NA;
③尾气中NO、NO2与石灰乳反应生成Ca(NO2)2和水,反应方程式为:NO+NO2+Ca(OH)2═Ca(NO2)2+H2O;
(3)①阳极上氢氧根离子放电生成氧气和水,电极反应式为4OH--4e-═2H2O+O2↑;
②HCO3-存在电离平衡:HCO3-![]() H++CO32-,阴极H+放电浓度减小平衡右移,CO32-再生;阴极H+放电OH-浓度增大,OH-与HCO3-反应生成CO32-,CO32-再生;
H++CO32-,阴极H+放电浓度减小平衡右移,CO32-再生;阴极H+放电OH-浓度增大,OH-与HCO3-反应生成CO32-,CO32-再生;
③已知:H2(g)+1/2O2(g)═H2O(g)△H1=-242kJ/mol①
CH3OH(g)+3/2O2(g)═CO2(g)+2H2O(g)△H2=-676kJ/mol②
根据盖斯定律可知将方程式3×①-②得CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H=3×(-242kJ/mol)-(-676kJ/mol)="-50" kJ/mol。


科目:高中化学 来源: 题型:
【题目】铁、稀盐酸、澄清石灰水、氯化铜溶液是常见的物质,四种物质间的反应关系如图所示。图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是( )
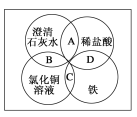
A.OH-+HCl===H2O+Cl-
B.Ca(OH)2+Cu2+===Ca2++Cu(OH)2
C.Fe+Cu2+===Cu+Fe2+
D.Fe+2H+===Fe3++H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,1 mol/L的NH4Cl、CH3COONH4、NH4HSO4、NH3·H2O四种溶液中,测得c(NH![]() )分别为a、b、c、d(单位为mol/L),下列判断正确的是( )
)分别为a、b、c、d(单位为mol/L),下列判断正确的是( )
A.a=b=c=d B.a>b>d>c
C.d >a>c>b D.c>a>b>d
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】丁二酮肟![]() 是检验Ni2+的灵敏试剂。
是检验Ni2+的灵敏试剂。
(1)Ni2+基态核外电子排布式为___________ 。丁二酮肟分子中C原子轨道杂类型为 ____________,1mol丁二酮肟分子所含![]() 键的数目为 ____________,分子中各原子的电负性由大到小的顺序为______________。
键的数目为 ____________,分子中各原子的电负性由大到小的顺序为______________。
(2)Ni能与CO形成四羰基镍[Ni(CO)4],四羰基镍熔点-19.3℃,沸点42.1℃,易溶于有机溶剂。
①Ni(CO)4固态时属于 __________晶体(填晶体类型)。
②与CO互为等电子体的阴离子为 ________________(填化学式)。
(3)Ni2+与Mg2+、O2—形成晶体的晶胞结构如图所示(Ni2+未画出),则该晶体的化学式为 ____________。
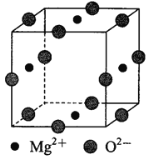
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有一份含有FeCl3和FeCl2固体的混合物,为测定FeCl2的含量,进行如下实验:
①称取混合物样品的质量7.06g,将样品溶解
②向溶解后的溶液中,加入足量的双氧水
③再向②所得溶液中加入足量的NaOH溶液,得到红褐色沉淀
④将沉淀过滤、洗涤后,加热灼烧,到质量不再减少,得到固体物质4.00g
根据实验回答下列问题:
(1)样品溶解过程中需加入 ,以防止 ;
(2)写出溶解后的溶液与双氧水反应的离子方程式 ;
(3)过滤操作中除用漏斗外,还需要的玻璃仪器有 ;
(4)简述检验实验步骤④中沉淀已经洗涤干净的方法 ;
(5)通过实验所得数据,计算固体样品中FeCl2的质量分数: ;
(6)实验室采用如图装置制取少量无水FeCl3固体.(已知FeCl3固体易潮解,部分夹持仪器已略去.)
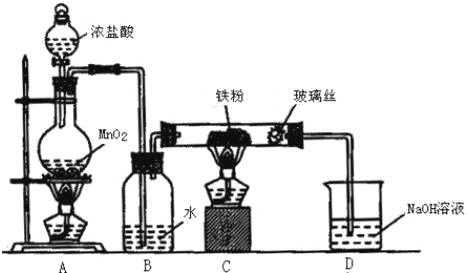
该装置存在明显缺陷,得不到无水FeCl3固体,请你对该装置进行合理的改进: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化能体现物质的漂白性的是:
A. SO2使酸性KMnO4溶液褪色 B. 乙烯使澳水褪色
C. Na2O2使无色酚酞先变红,后褪色 D. SO2使NaOH酚酞溶液褪色
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com