
 ij��ѧ��ȤС����100mL 1mol/L NaOH��Һ��ȫ������a mol CO2��õ���ҺA��Һ������ޱ仯����Ϊ��ȷ����ҺA�����ʳɷּ�aֵ������ȤС���ͬѧ����������ʵ�飮������������������Ӧʵ�����ݣ�
ij��ѧ��ȤС����100mL 1mol/L NaOH��Һ��ȫ������a mol CO2��õ���ҺA��Һ������ޱ仯����Ϊ��ȷ����ҺA�����ʳɷּ�aֵ������ȤС���ͬѧ����������ʵ�飮������������������Ӧʵ�����ݣ����� ��100mL 1mol/L NaOH��Һ��ȫ������a mol CO2��õ���ҺA��Һ������ޱ仯����������̼������������Һ��Ӧ����̼���ƣ���Һ��Ϊ�������ƺ�̼���ƣ�������̼ǡ�ú�����������Һ��Ӧ����̼���ƣ�������̼���˵õ���Һ������Ϊ̼���ƺ�̼�����ƣ�������̼������Ӧ����̼�����ƣ�
��2����ͬѧȡ������ҺA���Թܣ������Թ��еμӼ��η�̪��Һ����ҺA��죬��Һ�ʼ��ԣ����ܵ�ԭ���Ǽ���������������̼������Һ��̼������ӡ�̼���������ˮ����Һ�Լ��ԣ�����һ�������Ӧ��ȡ������Һ�������м����������Ȼ�����Һ���۲쵽��ҺA�������Ϊ�˼�����ҺA�к���̼���ƣ�
��3����ͬѧ���û�����Һ���й��ˣ�������Һ��Ϊ���ݣ������е�һ�ݼ���ϡ���ᣬ����ɫ�������ɣ���̼��������Һ�����ᷴӦ���ɶ�����̼���壬����̼���ƺ�̼�����ƣ�
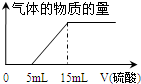
��4��ͼ�������֪��ʼ������������5ml�����ɶ�����̼������������Ϊ10ml��������ӦΪ��2Na2CO3+H2SO4=2NaHCO3+Na2SO4��2NaHCO3+H2SO4=Na2SO4+2CO2��+2H2O֤����������Ϊ�����ʵ�����̼���ƺ�̼�����ƣ����ݻ�ѧ����ʽ������ϵ����õ���
��� �⣺��100mL 1mol/L NaOH��Һ��ȫ������a mol CO2��õ���ҺA��Һ������ޱ仯����������̼������������Һ��Ӧ����̼���ƣ���Һ��Ϊ�������ƺ�̼���ƣ�������̼ǡ�ú�����������Һ��Ӧ����̼���ƣ�������̼���˵õ���Һ������Ϊ̼���ƺ�̼�����ƣ�������̼������Ӧ����̼�����ƣ��������ҺA������ΪNaOH��Na2CO3���������ҺA������ΪNa2CO3���������ҺA������ΪNa2CO3��NaHCO3�����������ҺA������ΪNaHCO3��
�ʴ�Ϊ��NaHCO3��
��2����ͬѧȡ������ҺA���Թܣ������Թ��еμӼ��η�̪��Һ����ҺA��죬��Һ�ʼ��ԣ����ܵ�ԭ���Ǽ���������������̼������Һ��̼������ӡ�̼���������ˮ����Һ�Լ��ԣ������ӷ���ʽ˵����ͬѧ���ж�����Ϊ��CO32-+H2O?HCO3-+OH- ��HCO3-+H2O?H2CO3+OH-������һ�������Ӧ��ȡ������Һ�������м����������Ȼ�����Һ���۲쵽��ҺA�������Ϊ�˼�����ҺA�к���̼���ƣ�
�ʴ�Ϊ��CO32-+H2O?HCO3-+OH- ��HCO3-+H2O?H2CO3+OH-��BaCl2��Na2CO3��
��3����ͬѧ���û�����Һ���й��ˣ�������Һ��Ϊ���ݣ������е�һ�ݼ���ϡ���ᣬ����ɫ�������ɣ���̼��������Һ�����ᷴӦ���ɶ�����̼���壬����̼���ƺ�̼�����ƣ��������ȷ��
�ʴ�Ϊ����
��4��ͼ�������֪��ʼ������������5ml�����ɶ�����̼������������Ϊ10ml��֤����������Ϊ�����ʵ�����̼���ƺ�̼�����ƣ����ݻ�ѧ����ʽ������ϵ����õ���������Ũ��Ϊ��cmol/L��������ӦΪ��2Na2CO3+H2SO4=2NaHCO3+Na2SO4��2NaHCO3+H2SO4=Na2SO4+2CO2��+2H2O��
����Ԫ���غ���ʽ���㣺100mL 1mol/L NaOH��Һn��NaOH��=0.1mol��ȡ10ml��Һ�к��������������ʵ���Ϊ0.01mol������Ũ��Ϊc��
�õ�0.015L��c��2=0.01mol
c=$\frac{1}{3}$mol/L������ͼ���֪NaHCO3��������10ml��
2NaHCO3+H2SO4=Na2SO4+2CO2��+2H2O
2 1
n �� 0.015L-0.005L����$\frac{1}{3}$
n=$\frac{0.02}{3}$mol
100ml��Һ������̼�غ�õ�������̼���ʵ���a=$\frac{0.02}{3}$mol��10=$\frac{1}{15}$mol��
�ʴ�Ϊ��$\frac{1}{15}$mol��$\frac{1}{3}$mol/L��
���� ���⿼����������ɵ�ʵ��̽���������������ʵ�����Ӧ�ã����ջ����ǹؼ�����Ҫ��̼���Ƶ�����ˮ�ķ�Ӧ���̷����жϣ���Ŀ�Ѷ��еȣ�


 ��ѧ����ͬ����ϰϵ�д�
��ѧ����ͬ����ϰϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ʹ��̪��Һ������Һ��Na+��Cl-��SO42-��Fe3+ | |
| B�� | ��ˮ�����c��H+��=10-12 mol•L-1����Һ��K+��Ba2+��Cl-��Br- | |
| C�� | ��pH=1����Һ�У�NH4+��K+��NO3-��Cl- | |
| D�� | ��NO3-���ڵ�ǿ������Һ�У�NH4+��Ba2+��Fe2+��Br- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C | B�� | H2O | C�� | H2 | D�� | CO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �Ҵ����ױ��������Ʒ�Ӧ�������� | |
| B�� | �춡�������黥Ϊͬ���칹�� | |
| C�� | ��֬�������ʾ����ڸ߷��ӻ����� | |
| D�� | ��ϩ�ͼ������������Ȼ�̼��Һ���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 4X | B�� | 3X | C�� | X | D�� | 0.5X |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com