
����Ŀ���⻯����һ����ɫ���塣������ˮ��ʵ�����Ʊ�KI����IJ�������:
I.����ͼ��ʾ��������ƿ�м���127g��ϸ�ĵ���I2��195g30%KOH��Һ������(��֪:I2��KOH��Ӧ����֮һ��KIO3)��
II.����ȫ��Ӧ��Һ©���еĻ��������ɼУ���װ��C��ͨ��������H2S��
III.��Ӧ��������װ��C�м���ϡH2SO4�ữ,ˮԡ���ȣ�
IV.��ȴ�����˵�KI����Һ��
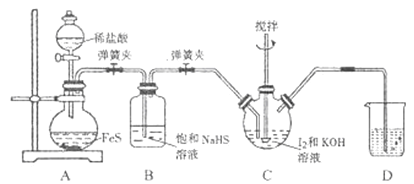
(1)���װ��A�����Եķ�����______������I����KOH��Һ������Ŀ����______��
(2)װ��B��������______��װ��D��ʢ�ŵ���Һ��______ ��
(3)д��װ��C��H2S��KIO3��Ӧ�����ӷ���ʽ: ______ ��
(4)����III��ˮԡ���ȵ�Ŀ���dz�ȥ______ (�ѧʽ)��
(5)�ɲ���IV���õ�KI����Һ(��SO42-)�Ʊ�KI�����ʵ�鷽��:�߽��������Һ�м���������______ (�ѧʽ����ͬ),��ֽ��衢���ˡ�ϴ�Ӳ������,����Һ��ϴ��Һ�ϲ�,����HI��Һ����������,�ڲ��Ͻ������������϶��������,ֹͣ����,����������,�õ�KI���塣�ڲⶨ��Ʒ��KI����ʱ,����京��Ϊ101.5%,��ԭ������Dz�Ʒ�к���______��
���𰸡� ��Һ©��ע��ˮ��,�رյ��ɼ�,��Һ©������ʹҺ�����£�һ��ʱ���Һ�岻��˳������,˵������������ ȷ�����ַ�Ӧ ��ȥH2S�����е�HCl ����������Һ IO3-+3H2S=3S��+I-+3H2O H2S BaCO3 I2(��KI3)
��������(1)���Aװ�õ������Է���Ϊ����Һ©��ע��ˮ�����رյ��ɼ�����Һ©������ʹҺ�����£�һ��ʱ���Һ�岻��˳��������˵�����������ã�KOH��Һ�����ɱ�֤I2���ʳ�ַ�Ӧ����߲��ʣ��ʴ�Ϊ��ȷ�����ַ�Ӧ��
(2)�����ӷ�������NaHS��Һ��������HCl���岢ͬʱ����H2S���壬��B�������dz�ȥH2S�����е�HCl��H2S�����ж���Ⱦ��������D��ʢ�ŵ���NaOH��Һ����ȥ������H2S���塣
(3) H2S���л�ԭ�ԣ�KIO3���������ԣ����߷���������ԭ��Ӧ��IO3-����ԭΪI-�����ӷ���ʽΪ��IO3-+3H2S=3S��+I-+3H2O��
(4) ����III����Һ�к�������ˮ��H2S��ˮԡ���ȿ��Խ�H2S�ϳ����������ʣ��ʴ�Ϊ������III��ˮԡ���ȵ�Ŀ���dz�ȥH2S��
(5)KI�к���K2SO4�����Լ��벻����ˮ��BaCO3���彫SO42-ת��ΪBaSO4������K2CO3��Ȼ���������HI�ٽ�CO32-��ȥ���ʴ�ΪBaCO3���ⶨ��Ʒ��KI����ʱ��KI�ĺ���ƫ�ߣ������Ǽ��ȹ����У�����I-������ΪI2���ʣ�����ΪI2+KI=KI3��I2���ʻ�KI3���ڲ�Ʒ�У����µ�Ԫ�غ������Ӷ�KI�ĺ���ƫ�ߣ��ʴ�ΪI2(��KI3)��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ3X(g)+Y(g)![]() 2Z(g)+2W(g)��2L�ܱ������н��У�5min��Y������0.5mol����˷�Ӧ��ƽ��������Ϊ( )
2Z(g)+2W(g)��2L�ܱ������н��У�5min��Y������0.5mol����˷�Ӧ��ƽ��������Ϊ( )
A. ��(X)��0.05mol��L��1��min��1 B. ��(Y)�� 0.10mol��L��1��min��1
C. ��(Z)��0.10mol��L��1��min��1 D. ��(W)��0.05mol��L��1��s��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ�̶��ݻ����ܱ������н��з�Ӧ��2SO2(g)+O2(g) ![]() 2SO3(g)����֪��Ӧ���е�10��ʱ��SO2��O2��SO3�����ʵ����ֱ�Ϊ0.2mol��0.1mol��0.2mol��������˵����ȷ����
2SO3(g)����֪��Ӧ���е�10��ʱ��SO2��O2��SO3�����ʵ����ֱ�Ϊ0.2mol��0.1mol��0.2mol��������˵����ȷ����
A .10��ʱ����O2��ʾ�÷�Ӧ��ƽ����Ӧ����Ϊ0.01mol/(L��s)
B������Ӧ�ﵽƽ��ʱ��SO3�����ʵ�������Ϊ0.4mol
C����SO2��O2����������֮��Ϊ2:1ʱ���ﵽ�÷�Ӧ��
D���������ڳ���SO2��������߷�Ӧ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ç��������ںϳ�ҩ���ƣ���ṹ��ʽ����ͼ�����й���ç�����˵����ȷ����
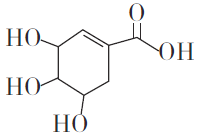
A. ����ʽΪC7H6O5
B. �ɷ����ӳɺ�ȡ����Ӧ
C. �����к������ֹ�����
D. 1molç������������Na��Ӧ�����ɱ�״����33.6L��H2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NA��������٤������������˵������ȷ���ǣ������� �ٳ��³�ѹ�£�17g������14CH3��������������Ϊ9NA
�ڳ��³�ѹ�£�22.4L NO����ķ�����С��NA
�������£�28.0g��ϩ�ͱ�ϩ�Ļ�������к��еĹ��ۼ�ԼΪ3��6.02��1023��
��7.2g CaO2�к��е���������ĿԼΪ6.02��1022
�ݱ�״��ʱ��22.4L�����������е�ԭ����Ϊ2NA
�ޱ���£�7.8g���к���̼̼˫������ĿΪ0.3NA ��
A.�٢ڢ�
B.�ڢܢ�
C.�ڢ�
D.�ݢ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���¶��£����ݻ�Ϊ2 L�����������н���ijһ��Ӧ��������M��N������������ʵ�����ʱ��ı仯������ͼ��ʾ����ͼ��֪

A. �÷�Ӧ�Ļ�ѧ����ʽΪN(g) ![]() 2M(g) B. t1��t2ʱ���ڣ�v(M)=(1/t2-t1) mol��L-1��min-1
2M(g) B. t1��t2ʱ���ڣ�v(M)=(1/t2-t1) mol��L-1��min-1
C. t2ʱ�����淴Ӧ������ȣ���Ӧ��ƽ��״̬ D. ƽ��ʱ������N��ת����Ϊ75%
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Ҫ������
��1�������к�����ߵ�Ԫ��Ϊ����Ԫ�ط��ţ���
��2�����������е�һ��������С��Ԫ�ص�����������ˮ����ĵ���ʽΪ ��
��3���縺������Ԫ�ص�ԭ�Ӻ�������Ų�ʽΪ ��
��4���ڶ������У���һ�����ܽ���B��N֮���Ԫ�ع����֣�
��5�����������Ų�Ϊ4s24p1��ԭ�ӵĺ˵����Ϊ
��6��ǰ36��Ԫ���У�δ�ɶԵ���������Ԫ�������ڱ��е�λ��Ϊ �� ��λ�� ����
��7�������ϵ�Ԫ�ؾ�������ǽ������ǽ��� ������ϡ�����壩��Ӧ �֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼͼ���У�������Ϊ����������ʵ�����������Ϊ����Һ�м��뷴Ӧ������ʵ���������Ӧ��ͼ������루1������4����Ӧ���� 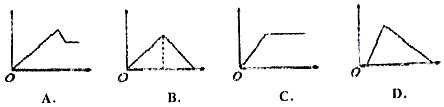
��Һ | �������� | ��Ӧ��ͼ�� |
�ű���ʯ��ˮ | ͨ����CO2���� | |
���Ȼ�����Һ | ���������ˮ | |
��MgCl2��AlCl3�Ļ��Һ | ��μ���NaOH��Һ������ | |
�Ⱥ�����NaOH��NaAlO2��Һ | ��μ���ϡ���� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com