
��6�֣���ϡ������Ԫ��Xe��믣��γɵ�һ�ֹ��ۻ�����XeO3�����ȶ�����ת��Ϊ���ʶ���ǿ�����ԡ���������XeO3Ͷ��30 mL Mn2+Ũ��Ϊ0.1 mol��L-1��ˮ��Һ�У��պ���ȫ��Ӧ���ų���Ψһ������Xe���ʣ����ڱ�״���µ����Ϊ56 mL���ڷ�Ӧ��������Һ��pH���ϼ�С��
��1����֪Mn2+�ڲ�ͬ�����£��ɱ�����Ϊ+4��+6��+7�Ȳ�ͬ��̬��������Ŀ����������������������������Ԫ�صĻ��ϼ�Ϊ____________��
��2����д���йص����ӷ���ʽ��________________��
��3��������Ӧ�����Һϡ����90 mL����ϡ�ͺ���Һ��pHΪ____________��
��6�֣���1��+7 ��2��5XeO3+6Mn2++9H2O=5Xe+6 MnO4-+18H+ ��3��1
��������
�����������1��XeO3��Xe�Ļ��ϼ���+6�ۣ������е�Xe�Ļ��ϼ���0�ۣ����ϼ۽��ͣ�����MnԪ�صĻ��ϼ�Ӧ�����ߣ�56 mLXe�����ʵ�����0.056L/22.4L/mol=0.025mol����ת�Ƶ��ӵ����ʵ�����0.025mol��6=0.015mol��Mn2+�����ʵ�����0.03L��0.1 mol��L-1=0.003mol����MnԪ�����ߺ�Ļ��ϼ���x�����ݵ�ʧ�����غ��0.015=0.003��x-2����x=7������������������Ԫ�صĻ��ϼ�Ϊ+7�ۣ�
��2��XeO3��Mn2+��Ӧ��IJ�������Xe���ʣ�+7��Mn��Ӧ��������MnO4-����Ӧ��������Һ��pH���ϼ�С��˵�������������ɣ����Է�Ӧ�����ӷ���ʽΪ5XeO3+6Mn2++9H2O=5Xe+6 MnO4-+18H+ ��
��3��Mn2+�����ʵ�����0.03L��0.1 mol��L-1=0.003mol�������������ӵ����ʵ�����0.009mol���������ӵ�Ũ��Ϊ0.009mol/0.09L=0.1mol/L,������Һ��pH=1.
���㣺����������ԭ��Ӧ���ж����������



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ѧ�ڻ�ͷ���Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�ȼҵ�IJ���NaOH�벻ͬ���ʷ�Ӧ�������ɲ�ͬ���Ρ���֪�����£�Ũ�Ⱦ�Ϊ0.1 mol/L��4��������ҺpH���±���
���� | Na2CO3 | NaHCO3 | NaClO | NaHSO3 |
pH | 11.6 | 9.7 | 10.3 | 5.2 |
����˵���У� ��ȷ����( )
A������ˮ�м���NaHCO3������������ˮ�д������Ũ��
B��������Һ�У�ˮ�ĵ���̶�������NaClO
C�������£���ͬ���ʵ���Ũ�ȵ�H2SO3��H2CO3��HClO��pH������H2SO3
D��NaHSO3��Һ������Ũ�ȴ�С˳��Ϊc��Na+��> c��H+��>c��HSO3-�� >c��SO32-��>c��OH-��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ʮУ�����������һ��������ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵���������
A����ѧ���Ķ��Ѻ��γ��ǻ�ѧ��Ӧ�������仯����Ҫԭ��
B�����ȷ�Ӧ�����ȷ�Ӧ�����ڷ�Ӧ����������������������������Դ�С
C����ѧ��Ӧ�������仯,ͨ����Ҫ����Ϊ�����ı仯------���Ȼ�������
D���������ȶ������Ļ�ѧ��Ӧ�������ȷ�Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ʮУ�����������ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
X��Y��Z��W���ֶ�����Ԫ�������ڱ��е����λ������ͼ��ʾ������X��W��������֮��Ϊ21���ɴ˿�֪�� ��
| X |
| Y |
Z |
| W |
|
A��Xλ��Ԫ�����ڱ��е�2���ڡ���VA��
B��Y���⻯��(H2Y)���ȶ���100�����ϼ��ɷֽ�
C��Z������������ˮ������һ��ǿ��
D��W�ķǽ����Ա�Y�ķǽ�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ������ʮУ�����������ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
������������ȷ���У� ��
��NH4I�ĵ���ʽ��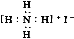
��8�����ӵ�̼ԭ�ӵĺ��ط��ţ�
�۵�ơ����ۡ�ˮ�������ײ��Ͼ�Ϊ����
���ռ�����ᡢ�ȷ¡�������Ϊ�����
����������ƽ��ȡ8.75gʳ��
������ʽ�ζ�����ȡ23.22mL���������Һ
��C60��C70�����ʯ��ʯī��Ϊ̼��ͬ��������
��X���ߡ����ס��˴Ź��������ִ���ѧ�����ʽṹ�����о����ֶ�
A��6�� B��5�� C��4�� D��3��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��λ�����ϡ��Һ�У��ǻӷ������ʵķ��ӻ�������Խ�࣬����Һ�ķе��Խ�ߣ���������Һ�е���ߵ���(����)
A��0.01 mol/L��������Һ B��0.01 mol/L��CaCl2��Һ
C��0.02 mol/L��NaCl��Һ D��0.02 mol/L��CH3COOH��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ����9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
����ͭ��������ӻ�ͭ��ʼ����ͭ���ڱ��չ�������Ҫ��Ӧ֮һ�Ļ�ѧ����ʽΪ
2CuFeS2��O2===Cu2S��2FeS��SO2����˵������ȷ����(����)
A��O2ֻ��������
B��CuFeS2�������������ǻ�ԭ��
C��SO2���������������ǻ�ԭ����
D������1 mol O2�μӷ�Ӧ����Ӧ�й���4 mol����ת��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ�����¿���10�£���ѧ�Ծ��������棩 ���ͣ�ѡ����
��4��ȼ�ϵ�أ�A ����������ȼ�ϵ�أ�B ��������ȼ�ϵ�أ�C ���ӽ���Ĥȼ�ϵ�أ�D ������ȼ�ϵ�ء������ǹ���ԭ��ʾ��ͼ������������Ӧ�IJ���Ϊˮ����

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015���㽭ʡ�����и���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
ij�������У����������õ���X2O72�����ӣ�����Һ��0.2 mol������ǡ����ʹ0.6molSO32��������ȫ��������X2O72�����ӻ�ԭ��Ļ��ϼ�Ϊ
A����1 B����2 C����3 D����4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com