
 某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )
某研究小组开发出一种人工仿生叶,据称该装置能“吃”进二氧化碳产出生物乙醇.这种装置能够利用太阳能电池板所提供的电力,而系统内的微生物以氢为食,能把空气中的二氧化碳转化为生物燃料.下列说法正确的是( )| A. | 该电池为原电池装置 | |
| B. | a与外接电源正极相连 | |
| C. | a电极的电极反应式为2CO2+6H++12e-═C2H5OH+3H2O | |
| D. | 当a电极上生成1 mol C2H5OH时,b电极上产生标准状况下的气体体积为67.2 L |
分析 A、整个过程是将太阳能转化为电能,然后电能转化为化学能;
B、a是发生还原反应,应与外接电源负极相连;
C、a电极的电极反应式为2CO2+12H++12e-═C2H5OH+3H2O;
D、当a电极上生成1 mol C2H5OH时,转移12mol的电子,所以b电极上产生标氧气为3mol.
解答 解:A、整个过程是将太阳能转化为电能,然后在装置中将电能转化为化学能,所以该电池为电解池装置,故A错误;
B、CO2→C2H5OH中碳的化合价降低,所以a是发生还原反应,应与外接电源负极相连,而不是与正极相连,故B错误;
C、a电极的电极反应式为2CO2+12H++12e-═C2H5OH+3H2O,故C错误;
D、当a电极上生成1 mol C2H5OH时,转移12mol的电子,所以b电极上产生标氧气为3mol,标准状况下的气体体积为67.2 L,故D正确;
故选D.
点评 本题考查了电化学原理,明确电极的判断方法、电极反应式的书写即可分析解答本题,难度不大.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 物质的量浓度为0.5 mol/L的MgCl2溶液中,含有Cl-的数目为 NA | |
| B. | 0.2 mol Fe与足量水蒸气反应,生成的H2分子数目为0.3 NA | |
| C. | 标准状况下,22.4LH2O含有的分子数为NA | |
| D. | 一定条件下2.3gNa与一定量氧气反应生成Na2O和Na2O2的混合物,转移的电子数一定为0.1NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 氧化亚铁溶于稀硝酸:FeO+2H+═Fe2++H2O | |
| B. | 往CaCl2溶液中通入少量的CO2:Ca2++CO2+H2O=CaCO3↓+2H+ | |
| C. | 碳酸氢铵溶液中加入过量氢氧化钠溶液:HCO3-+OH-=CO32-+H2O | |
| D. | 向澄清石灰水中滴加少量的NaHCO3溶液:Ca2++OH-+HCO3-=CaCO3↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 对环境的影响(或用途) | 解释 |
| A | 酒精用于环境消毒 | 酒精能使蛋白质变性 |
| B | 热碳酸钠溶液清除炊具上残留的油污 | 碳酸钠溶液水解显碱性 |
| C | SO2和NO2溶于水形成酸雨 | SO2和NO2是酸性氧化物 |
| D | 浸泡过酸性KMnO4溶液的硅藻土保鲜水果 | 酸性KMnO4溶液氧化乙烯 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
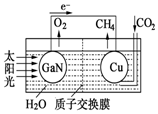 科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.
科学家用氮化镓材料与铜组装如图的人工光合系统,利用该装置成功地实现了以CO2和H2O合成CH4.查看答案和解析>>
科目:高中化学 来源: 题型:多选题
 500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )
500℃、20MPa时,将H2和N2置于一容积为2L的密闭容器中发生反应:3H2+N2?2NH3△H<0.反应过程中H2、N2和NH3物质的量变化如图所示,据图判断下列叙述不正确的是( )| A. | 从曲线变化可以看出,反应进行到10min至20min时可能采取的措施是使用了催化剂 | |
| B. | 25min时平衡正向移动但达到新平衡后 NH3的体积分数比原平衡大 | |
| C. | 反应开始到第一次平衡时,N2的平均反应速率为0.0625mol•(L•min)-1,H2的转化率为75% | |
| D. | 从曲线变化可以看出,反应进行至25min时,采取的措施是分离出0.1mol的氨气,平衡正向移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
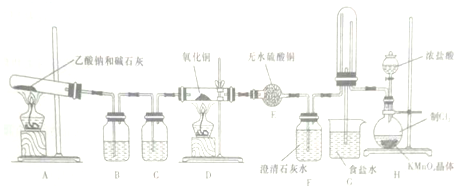
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com