
| 1 |
| 2 |
| 1 |
| 2 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| 化学反应 | 平衡常数 | 温度℃ | |
| 500 | 800 | ||
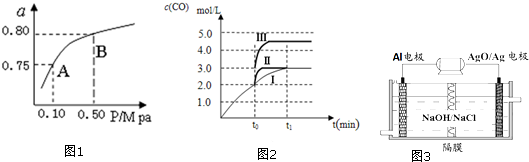
| ①2H2(g)+CO(g)?CH3OH(g) | K1 | 2.5 | 0.15 |
| ②H2(g)+CO2(g)?H2O (g)+CO(g) | K2 | 1.0 | 2.50 |
| ③3H2(g)+CO2(g)?CH3OH(g)+H2O (g) | K3 | ||
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、欲提高氯水中HClO的浓度可往氯水加适量的碳酸钙粉末 |
| B、形成酸雨的氧化物主要是SO2和氮的氧化物,CO2是造成温室效应的主要气体 |
| C、水晶项链和餐桌上的瓷盘都是硅酸盐制品 |
| D、大气中的N2可转化为NO,NO可转化为NO2、硝酸等;含硫物质在自然界中可转化为SO2等含硫化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氧化剂与还原剂的物质的量之比为1:8 |
| B、若有1mol NO3-被还原,转移8 mol e- |
| C、还原产物为NH4+ |
| D、若把该反应设计为原电池,则正极反应为Fe2+-e-=Fe3+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、NaNO2溶液中加入酸性KMnO4溶液:2MnO4-+5NO2-+6H+=2Mn2++5NO3-+3H2O |
| B、碳酸氢铵溶液中加入足量氢氧化钡溶液:NH4++HCO3-+2OH-=CO32-+NH3?H2O+H2O |
| C、用食醋和淀粉-KI试纸检验碘盐中的KIO3:IO3-+5I-+6H+=I2+3H2O |
| D、用惰性电极电解熔融氯化钠:2Cl-+2H2O=Cl2↑+H2↑+2OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、强电解质全部是离子化合物 |
| B、强电解质在水中的溶解度一定大于弱电解质 |
| C、强电解质在水溶液中完全电离 |
| D、强电解质溶液的导电能力一定强于弱电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
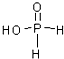 ,是一种精细化工产品,是一元中强酸,具有较强还原性.回答下列问题:
,是一种精细化工产品,是一元中强酸,具有较强还原性.回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.012 kg12C含有6.02×1023个碳原子 |
| B、1 mol任何物质都含有6.02×1023个原子 |
| C、硫酸的摩尔质量是98 g |
| D、常温常压下,1 mol氧气的体积为22.4 L |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com