
”¾ĢāÄæ”æSCR¼¼ŹõæÉÓŠŠ§½µµĶ²ńÓĶ·¢¶Æ»śĪ²ĘųÖŠNOxµÄÅÅ·Å”£SCR£ØŃ”ŌńŠŌ“߻ƻ¹Ō£©¹¤×÷ŌĄķČēĶ¼ĖłŹ¾”£
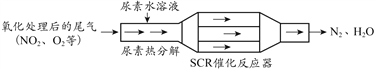
£Ø1£©Ęū³µĪ²ĘųÖ±½ÓÅÅ·Å»įŌģ³É_______
a. ĻõĖįŠĶĖįÓź b. ĮņĖįŠĶĖįÓź c. ³ōŃõ²ćæÕ¶“
£Ø2£©ÄņĖŲ[CO(NH2)2]Ė®ČÜŅŗČČ·Ö½āĪŖNH3ŗĶCO2£¬·“Ó¦Ę÷ÖŠNH3æÉŅŌ»¹ŌNO2£¬Ęšµ½×Ŗ»ÆÓŠŗ¦ĪļÖŹĪŖĪŽŗ¦ĪļÖŹµÄ×÷ÓĆ£¬ŅŃÖŖ²Ī¼Ó·“Ó¦µÄ°±ĘųÓėNO2µÄĢå»ż±ČĪŖ£“:£³£¬Ęä·“Ó¦·½³ĢŹ½ĪŖ_________”£
£Ø3£©øł¾ŻŌŖĖŲŹŲŗć£¬×īÖÕ“¦Ąķ²śĪļ³żĮĖN2ŗĶH2O£¬»¹ÓŠ_______”£
£Ø4£©ČōĶØČėĪ²ĘųÖŠŗ¬67.2L NO2£Ø±ź×¼×“æö£©£¬ŌņÓė°±ĘųĶźČ«·“Ó¦×ŖŅʵē×ÓŹżĪŖ_____mol”£
”¾“š°ø”æ a £ØacŅ²øų·Ö£© 8NH3+6NO2==7N2+12H2O CO2 12
”¾½āĪö”æ£Ø1£©a”¢Ęū³µĪ²ĘųÖŠµŖµÄŃõ»ÆĪļÖ±½ÓÅÅ·Å»įÓėæÕĘųÖŠµÄŃõĘųŗĶĖ®×÷ÓĆÉś³ÉĻõĖįŌģ³ÉĻõĖįŠĶĖįÓź£¬¹ŹaÕżČ·£»b”¢Ęū³µĪ²ĘųÖŠŗ¬ĮņĪļÖŹŗÜÉŁ£¬¹Ź²»»įŠĪ³ÉĮņĖįŠĶĖįÓź£¬¹Źb“ķĪó£»c”¢µŖµÄŃõ»ÆĪļÖ±½ÓÅŷŵ½æÕĘųÖŠ£¬Ņ²»į¶Ō³ōŃõ²ć²śÉśĘĘ»µ×÷ÓĆ£¬¹ŹcÕżČ·£»¹ŹŃ”a»ņac”££Ø2£©°±ĘųÓėNO2µÄĢå»ż±ČĪŖ£“:£³£¬Ęä·“Ó¦·½³ĢŹ½ĪŖ8NH3+6NO2==7N2+12H2O£»£Ø3£©øł¾ŻŌŖĖŲŹŲŗć£¬ĘūÓĶÖŠC”¢H”¢OŗĶæÕĘųÖŠµŖ£¬×īÖÕ“¦Ąķ²śĪļ³żĮĖN2ŗĶH2O£¬»¹ÓŠCO2£»£Ø4£©ČōĶØČėĪ²ĘųÖŠŗ¬67.2L NO2£Ø±ź×¼×“æö£©£¬n( NO2)=67.2L/22.4L”¤mol£1=3mol£¬ÓÉ8NH3+6NO2==7N2+12H2O£¬Ćæ6molNO2·“Ó¦×ŖŅĘ24molµē×Ó£¬Ōņ3molNO2Óė°±ĘųĶźČ«·“Ó¦×ŖŅʵē×ÓŹżĪŖ12mol”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ±½ŌŚČ¼ÉÕŹ±²»æÉÄÜÉś³ÉµÄŹĒ£Ø £©
A.¶žŃõ»ÆĢ¼
B.Ė®
C.ĀČ»ÆĒā
D.Ņ»Ńõ»ÆĢ¼
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠ¹ŲÓŚæÕĘųÖŠµÄµŖŃ»·£¬Ėµ·Ø²»ÕżČ·µÄŹĒ
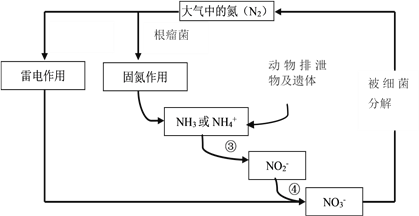
A. µŖŌŖĖŲ¾ł±»Ńõ»Æ
B. Ö²ĪļæÉŅŌ¹ĢµŖ
C. Ģ¼ĒāŃõŅ²²ĪÓėĮĖµŖŃ»·
D. ŗ¬µŖ»ÆŗĻĪļ¶ŌČĖĄąÓŠ¾Ž“ó×÷ÓĆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ£Ø1£©ŌŚ3ÖÖÓŠ»śĪļ ¢Ł ![]() ”¢¢Ś CH2£½CH2”¢¢ŪĘĻĢŃĢĒÖŠ£¬“ÓŹÆÓĶÖŠĢįČ”µÄÖŲŅŖÓŠ»śČܼĮŹĒ______£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£¬æÉÓĆ×÷Éś²śĖÜĮĻ“üµÄŹĒ_______”£ĪŖČĖĢåĢį¹©ÄÜĮæµÄĪļÖŹŹĒ_______”£
”¢¢Ś CH2£½CH2”¢¢ŪĘĻĢŃĢĒÖŠ£¬“ÓŹÆÓĶÖŠĢįČ”µÄÖŲŅŖÓŠ»śČܼĮŹĒ______£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£¬æÉÓĆ×÷Éś²śĖÜĮĻ“üµÄŹĒ_______”£ĪŖČĖĢåĢį¹©ÄÜĮæµÄĪļÖŹŹĒ_______”£
£Ø2£©ŌŚ3ÖÖĪŽ»śĪļ ¢Ł Na2SiO3”¢¢ŚHNO3”¢¢Ū SO2ÖŠ£¬æÉÓĆ×÷×čČ¼µÄŹĒ______£ØĢīŠņŗÅ£¬ĻĀĶ¬£©£¬æÉÓĆÓŚĘÆ°×ÖÆĪļµÄŹĒ______£¬ æÉÓĆ×÷Éś²śÕØŅ©µÄŹĒ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓŠŅ»°üĀČ»ÆŃĒĢśŃłĘ·£¬ĘäÖŠ»ģÓŠÉŁĮæµÄAlCl3”¢FeCl3µČŌÓÖŹ£¬Ä³Š”×éĪŖĮĖĢį“æĀČ»ÆŃĒĢś£¬½ųŠŠĮĖČēĻĀŹµŃ锣

£Ø1£©²½ÖčiiµÄÄæµÄŹĒ____________£¬ĘäĄė×Ó·½³ĢŹ½ĪŖ____________”£
£Ø2£©ČÜŅŗCÖŠŅõĄė×ÓÓŠ____________£¬·“Ó¦iiiµÄĄė×Ó·“Ó¦·½³ĢŹ½ĪŖ____________”£
£Ø3£©øł¾ŻÉĻŹöŹµŃ飬ĻĀĮŠÄÄÖÖĖµ·ØŹĒ²»ŗĻĄķµÄ_______
¢ŁČÜŅŗBÖŠŗ¬ÓŠ½šŹōĄė×ÓÖ»ÓŠĮ½ÖÖ
¢ŚČÜŅŗCÖŠÓŠĮ½ÖÖ½šŹōŃōĄė×Ó
¢Ū¹ĢĢåD¼ÓČČæÉ·Ö½ā
£Ø4£©øł¾ŻŃłĘ·µÄÖŹĮ棬Ŋ¶Ļ¼ÓČė1mol/L NaOHČÜŅŗµÄĢå»żŗĻĄķµÄĪŖ__________”£
¢Ł 40mL ¢Ś 400mL ¢Ū 4L
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ×ŌČ»½ēÖŠµÄĪļÖŹ¾ų“󶹏żŅŌ»ģŗĻĪļµÄŠĪŹ½“ęŌŚ£¬ĪŖĮĖ±ćÓŚŃŠ¾æŗĶĄūÓĆ£¬³£Šč¶Ō»ģŗĻĪļ½ųŠŠ·ÖĄėŗĶĢį“攣ĻĀĮŠA”¢B”¢C”¢DŹĒ֊ѧ³£¼ūµÄ»ģŗĻĪļ·ÖĄė»ņĢį“æµÄ×°ÖĆ”£

¢ń£®Ēėøł¾Ż»ģŗĻĪļ·ÖĄė»ņĢį“æµÄŌĄķ£¬»Ų“šŌŚĻĀĮŠŹµŃéÖŠŠčŅŖŹ¹ÓĆÄÄÖÖ×°ÖĆ”£½«A”¢B”¢C”¢DĢīČėŹŹµ±µÄæÕøńÖŠ”£
£Ø1£©Ģ¼ĖįøĘŠü×ĒŅŗÖŠ·ÖĄė³öĢ¼ĖįøĘ___________£»
£Ø2£©ĀČ»ÆÄĘČÜŅŗÖŠ·ÖĄė³öĀČ»ÆÄĘ___________£»
£Ø3£©·ÖĄėÖ²ĪļÓĶŗĶĖ®___________£»
£Ø4£©ŗ£Ė®µ»Æ___________£»
£Ø5£©ĀČ»ÆÄĘČÜŅŗÖŠ·ÖĄė³öĖ®___________£»
£Ø6£©³żČ„×ŌĄ“Ė®ÖŠµÄCl©µČŌÓÖŹ___________£»
£Ø7£©“ÓµāĖ®ÖŠ·ÖĄė³öI2___________”£
¢ņ£®µāĖ®ÖŠĢįČ”µāµ„ÖŹµÄ·½·ØČēĻĀ£ŗ
£Ø1£©ŻĶČ”·ÖŅŗ
¢ŁĻĀĮŠæÉ×÷ĪŖµāĖ®ÖŠĢįČ”µāµ„ÖŹŻĶČ”¼ĮµÄŹĒ___________”£
A£®¾Ę¾« B£®±½
¢Ś·ÖŅŗĀ©¶·ŌŚŹ¹ÓĆĒ°±ŲŠėĻČ___________”£
¢Ū²é׏ĮĻµĆÖŖ£ŗ¦Ń£ØH2O£©>¦Ń£Ø±½£©>¦Ń£Ø¾Ę¾«£©£¬ČōÓĆ¢ŁÖŠĖłŃ”ŻĶČ”¼ĮŻĶČ”µāĖ®ÖŠµÄµāµ„ÖŹ£¬·ÖŅŗŹ±£¬Ė®²ćÓ¦ÓÉ·ÖŅŗĀ©¶·µÄ______¶ĖæŚ·Å³ö£¬ÓŠ»ś²ćÓ¦ÓÉ·ÖŅŗĀ©¶·µÄ______¶ĖæŚ·Å³ö£Ø“ĖĪŹĢī”°ÉĻ”±»ņÕß”°ĻĀ”±£©
£Ø2£©ÕōĮó
¢Ł×°ÖĆAÖŠaµÄĆū³ĘŹĒ_______£¬ĄäÄż×°ÖĆÖŠĄäÄżĖ®Ó¦øĆ________æŚ½ų£ØĢī”°ÉĻ”±»ņ”°ĻĀ”±£©£¬ÕāŃł×öµÄÄæµÄŹĒ________________________£¬×°ÖĆCŌŚ·ÖŅŗŹ±ĪŖŹ¹ŅŗĢåĖ³ĄūµĪĻĀ£¬³ż“ņæŖĀ©¶·ĻĀ¶ĖµÄŠżČūĶā£¬»¹Ó¦½ųŠŠµÄ¾ßĢå²Ł×÷ŹĒ__________________________”£
¢ŚŅŃÖŖµāŗĶĖÄĀČ»ÆĢ¼µÄČŪ·ŠµćŹż¾ŻČēĻĀ±ķ
ČŪµć | ·Šµć | |
µā | 113.7”ę | 184.3”ę |
ĖÄĀČ»ÆĢ¼ | -22.6”ę | 76.8”ę |
ČōÓĆÕōĮó·Ø·ÖĄėµāŗĶĖÄĀČ»ÆĢ¼µÄ»ģŗĻĪļ£¬×¶ŠĪĘæÖŠĻČŹÕ¼Æµ½µÄĪļÖŹµÄĆū³ĘŹĒ___________”£
¢ó. ŗ£Ė®ÖŠŌĢ²Ų×Å·įø»µÄ׏Ō“£¬ŌŚŹµŃéŹŅ֊ȔɣĮæŗ£Ė®£¬½ųŠŠČēĻĀĮ÷³ĢµÄŹµŃé£ŗ

ĪŹĢāŅ»£ŗ“ÖŃĪÖŠŗ¬Ca2+”¢Mg2+”¢SO42©µČŌÓÖŹ£¬ŠčŅŖĢį“æŗó²ÅÄÜ×ŪŗĻĄūÓĆ”£“ÖŃĪĢį“æµÄ²½ÖčÓŠ£ŗ
¢Ł¼ÓČė¹żĮæµÄNa2CO3ČÜŅŗ””¢Ś¼ÓČė¹żĮæµÄBaCl2ČÜŅŗ””¢Ū¼ÓČė¹żĮæµÄNaOHČÜŅŗ””¢Üµ÷½ŚČÜŅŗµÄpHµČÓŚ7””¢ŻČܽā ¢Ž¹żĀĖ””¢ßÕō·¢ÕżČ·µÄ²Ł×÷Ė³ŠņŹĒ__________£ØĢīŃ”Ļī×ÖÄø£©.
¢Ż¢Ś¢Ū¢Ł¢Ž¢Ü¢ß b£®¢Ż¢Ł¢Ś¢Ū¢Ž¢Ü¢ß c£®¢Ż¢Ś¢Ł¢Ū¢Ü¢Ž¢ß d£®¢Ż¢Ū¢Ś¢Ł¢Ž¢Ü¢ß
ĪŹĢā¶ž£ŗÓÉŗ£Ė®µ½ĀČ»ÆÄĘ¾§ĢåµÄŹµŃé¹ż³ĢÖŠŅŖÓƵ½µÄÖ÷ŅŖ×°ÖĆŹĒ_________________£Ø“Óøų¶ØµÄĖÄÖÖ×°ÖĆÖŠŃ”Ōń£¬Ģī×ÖÄø£©”£
ĪŹĢāČż£ŗ“ÖŃĪÖŠŗ¬ÓŠÉŁĮæÄąÉ³”¢CaCl2”¢MgCl2¼°ĮņĖįŃĪ£¬½«“ÖŃĪČܽāŗó£¬ĻČ¹żĀĖ½«ÄąÉ³³żČ„£¬ŌŁ¼ģŃéĀĖŅŗÖŠµÄSO42©£¬¼ģŃéĀĖŅŗÖŠµÄSO42©µÄŹµŃé²Ł×÷ŗĶĻÖĻóŹĒ_________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŅŅĖį±½¼×õ„æÉĢįø߻ػņ¹ūµÄ·¼ĻćĘųĪ¶£¬¹Ź³£ÓĆÓŚ»Æױʷ¹¤ŅµŗĶŹ³Ę·¹¤Ņµ”£ŅŅĖį±½¼×õ„æÉŅŌÓĆĻĀĆęµÄÉč¼Ę·½°øŗĻ³É£ŗ
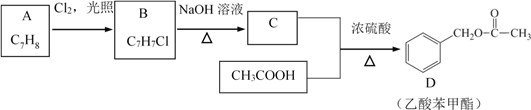
Ēė»Ų“š£ŗ
£Ø1£©ŅŅĖį±½¼×õ„ÖŠ¹ŁÄÜĶŵÄĆū³ĘŹĒ________”£
£Ø2£©Aµ½BµÄ·“Ó¦ĄąŠĶŹĒ________”£
£Ø3£©ÓÉCÉś³ÉDµÄ·“Ó¦·½³ĢŹ½ĪŖ________”£
£Ø4£©Āś×ćĻĀĮŠĢõ¼žµÄDµÄĶ¬·ÖŅģ¹¹ĢåĪŖ________”££ØŠ“³öŅ»ÖÖ¼“æÉ£©
¢Ł ÓėFeCl3ČÜŅŗ·“Ó¦ĻŌ×ĻÉ«
¢Ś 1mol DæÉŅŌÓė4mol H2·¢Éś¼Ó³É·“Ó¦
¢Ū DµÄŗĖ“Ź²ÕńĒāĘ×ÓŠĖÄ×é·å£¬·åĆ껿±ČĪŖ6:2:1:1
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ³£ĪĀĻĀ£¬0.2mol/LµÄŅ»ŌŖ¼īBOHÓėµČÅØ¶ČµÄHClČÜŅŗµČĢå»ż»ģŗĻŗó£¬ĖłµĆČÜŅŗÖŠ²æ·ÖĪ¢Į£×é·Ö¼°ÅضČČēĶ¼ĖłŹ¾£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ£Ø £©
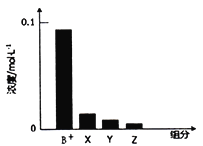
A. BOHĪŖĒæ¼ī B. øĆ»ģŗĻŅŗpH=7
C. Ķ¼ÖŠX±ķŹ¾BOH,Y±ķŹ¾H+,Z±ķŹ¾OH- D. øĆ»ģŗĻČÜŅŗÖŠ£ŗc(Cl-)=c(Y)+c(B+)
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ°“ŅŖĒó¶ŌĻĀĶ¼ÖŠĮ½¼«½ųŠŠ±ŲŅŖµÄĮ¬½Ó²¢ĢīæÕ£ŗ
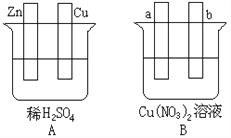
£Ø1£©ŌŚAĶ¼ÖŠ£¬Ź¹ĶʬÉĻĆ°ĘųÅŻ”£Ēė¼ÓŅŌ±ŲŅŖĮŖ½Ó£¬ŌņĮŖ½ÓŗóµÄ×°ÖĆ½Š_______________”£µē¼«·“Ó¦Ź½£ŗŠæµē¼«£ŗ________________________________£»Ķµē¼«£ŗ_____________________________”£
£Ø2£©ŌŚBĶ¼ÖŠ£Øa£¬b¶¼ĪŖ¶čŠŌµē¼«£©£¬Ź¹a¼«Īö³öĶ£¬ŌņbĪö³ö£ŗ_______________”£¼ÓŅŌ±ŲŅŖµÄĮŖ½Óŗó£¬øĆ×°ÖĆ½Š________________”£µē¼«·“Ó¦Ź½: b¼«£ŗ________________________________”£¾¹żŅ»¶ĪŹ±¼äŗó£¬Ķ£Ö¹·“Ó¦²¢½Į¾łČÜŅŗ£¬ČÜŅŗµÄpHÖµ____________£ØÉżøß”¢½µµĶ”¢²»±ä£©”£
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com