


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
| A.用溴水鉴别苯和溴苯 |
| B.用BaCl2溶液鉴别SO42—和CO32— |
| C.用浓HNO3和Cu反应制取NO |
| D.将混有HCl的Cl2通入饱和NaHCO3溶液中除去HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| | 试剂甲 | 离子X | 离子Y |
| A | HCl.Ba(OH)2 | CO32- | HCO3- |
| B | NH3 .H2O | Al3+ | Mg2+ |
| C | AgNO3 | I- | Cl- |
| D | NH4SCN,氯水 | Fe2+ | Fe3+ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.用图1所示装置除去HCl中含有的少量Cl2 |
| B.用图2所示装置蒸发FeCl3溶液制备无水FeCl3 |
| C.用图3所示装置可以完成“喷泉”实验 |
| D.用图4所示装置制取并收集干燥纯净的NH3 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

| A.水 | B.硫酸 | C.氢氧化钠溶液 | D.氯化锶饱和溶液 |
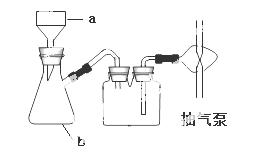
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
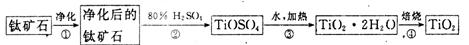
 TiCl4(1)+O2(g) △H=+151 kJ/mol。所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4,请说明判断该反应难以发生的理由是_______。当往氯化反应体系中加入碳后,反应在高温条件下能顺利进行生成TiCl4。
TiCl4(1)+O2(g) △H=+151 kJ/mol。所以不能直接由TiO2和Cl2反应(即氯化反应)来制取TiCl4,请说明判断该反应难以发生的理由是_______。当往氯化反应体系中加入碳后,反应在高温条件下能顺利进行生成TiCl4。 394 kJ/mol。
394 kJ/mol。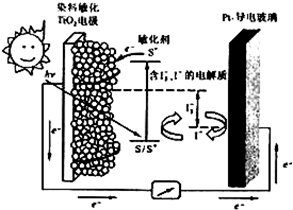
 TiO2/S*(激发态)
TiO2/S*(激发态) TiO2/S+ + e-
TiO2/S+ + e- 3I-
3I- 2TiO2/S + I3-
2TiO2/S + I3-| A.电池工作时,I-离子在镀铂导电玻璃电极上放电 |
| B.电池工作时,是将太阳能转化为电能 |
| C.电池的电解质溶液中I-和I3- 浓度不会减少 |
| D.电池中镀铂导电玻璃为正极 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.用装置①除去Cl2中含有的少量HCl |
| B.用装置②从氯化铁溶液中直接蒸发结晶获得无水氯化铁 |
| C.用装置③制取少量纯净的CO2气体 |
| D.用装置④分离CCl4萃取碘水后已分层的有机层和水层 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 被提纯的物质(杂质) | 除杂试剂 | 分离方法 |
| A | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| B | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 分液 |
| C | 乙醇(乙酸) | 新制生石灰 | 蒸馏 |
| D | 甲苯(苯酚) | 浓溴水 | 过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com