
 导学与测试系列答案
导学与测试系列答案 新非凡教辅冲刺100分系列答案
新非凡教辅冲刺100分系列答案科目:高中化学 来源:不详 题型:计算题
查看答案和解析>>
科目:高中化学 来源:不详 题型:计算题
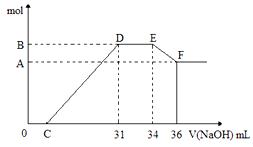
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
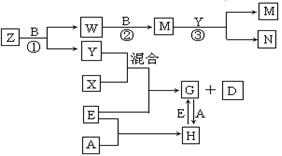
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是__________________。
2NH3(g)。在一定温度下,将一定量的N2和H2通入到体积为1L的密闭容器中达到平衡后.改变下列条件,能使平衡向正反应方向移动且平衡常数不变的是__________________。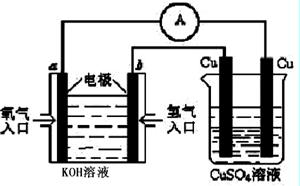
 H2(g) + CO(g) △H =" +131.3" kJ/mol
H2(g) + CO(g) △H =" +131.3" kJ/mol| A.△H >0 | B.温度较低时,△H影响为主 |
| C.△S<0 | D.温度较低时,△S影响为主 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
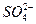 ====BaSO4↓来表示的是( )
====BaSO4↓来表示的是( )| A.Ba(NO3)2+H2SO4====BaSO4↓+2HNO3 |
| B.BaCO3+H2SO4====BaSO4↓+CO2↑+H2O |
| C.Na2SO4+BaCl2====BaSO4↓+2NaCl |
| D.BaCl2+H2SO4====BaSO4+2HCl |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.1.0 mol | B.1.6 mol | C.2.2 mol | D.2.4 mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com