
| A. | PCl3 | B. | H2O2 | C. | NO | D. | BF3 |
分析 分子中原子的最外层电子数可以根据每种元素原子的最外层电子数与化合价的绝对值之和来判断.
解答 解:A、PCl3中P元素化合价为+3,P原子最外层电子数为5,所以5+3=8,P原子满足8电子结构;Cl元素化合价为-1,Cl原子最外层电子数为7,所以1+7=8,Cl原子满足8电子结构,故A正确;
B、过氧化氢中的氢元素达到2电子稳定结构,故B错误;
C、一氧化氮中的氮元素,原子最外层电子数为5,所以5+2=7,故C错误;
D、BF3中,B元素位于第ⅢA族,则3+3≠8,不满足分子中所有原子都满足最外层8电子结构,故D错误;
故选A.
点评 本题考查原子的结构,本题中注意判断是否满足8电子结构的方法,注意利用化合价与最外层电子数来分析即可解答,明确所有原子都满足最外层8电子结构是解答的关键.


科目:高中化学 来源: 题型:实验题
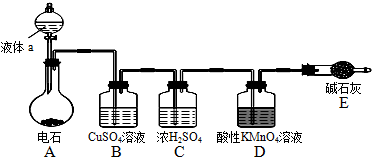
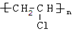 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数 | B. | 中子数 | C. | 质量数 | D. | 电子数 |
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 碳酸氢钠是焙制糕点的发酵粉的一种成分 | |
| B. | CO、NO、NO2都是大气污染物,在空气中都能稳定存在 | |
| C. | 光导纤维和玻璃都是硅酸盐产品 | |
| D. | 明矾能作净水剂,因为它能与水反应生成强氧化性的氢氧化铝胶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素编号 元素性质 | ① | ② | ③ | ④ | ⑤ |
| 原子半径/nm | 0.037 | 0.110 | 0.077 | 0.099 | 0.186 |
| 部分化合价 | +1 | -3+5 | -4+4 | -1 | +1 |
| A. | ④是周期表中非金属性最强的元素 | |
| B. | ①是周期表中原子半径最小的元素 | |
| C. | ②④⑤在位于同一个周期 | |
| D. | ①③两元素组成的最简单化合物分子与③④两元素组成的化合物分子空间构型相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.
某化学兴趣小组拟用如图装置制备氢氧化亚铁并观察其颜色.提供化学药品:铁屑、稀硫酸、氢氧化钠溶液.| 实验次数 | 第一次 | 第二次 | 第三次 |
| 消耗高锰酸钾溶液体积/mL | 25.52 | 25.02 | 24.98 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 如图所示的铜-锌原电池中,
如图所示的铜-锌原电池中,查看答案和解析>>
科目:高中化学 来源: 题型:填空题
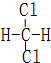 和
和 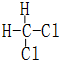 同一种物质.
同一种物质.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com