
将含O2和CH4的混合气体充入装有23.4gNa2O2的密闭容器中,点火花点燃,反应结束后,容器温度为150℃、压强为0 Pa。将残留物溶于水,无气体逸出。下列叙述正确的是( )
A.原混合气体中O2和CH4的体积比为2∶1;
B.原混合气体中O2和CH4的体积比为1∶2;
C.残留固体中有Na2CO3和NaOH;
D.残留固体中只有Na2CO3
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下面是某化学兴趣小组的同学做同周期元素性质递变规律实验时,设计了一套实验方案。其中实验步骤如下:
| 实验序号 | 实验步骤 |
| ① | 将镁条用砂纸打磨后,放入沸水中,再向溶液中滴加酚酞溶液 |
| ② | 向新制得到的Na2S溶液中滴加新制的氯水 |
| ③ | 将一小块金属钠放入滴有酚酞溶液的冷水中 |
| ④ | 将镁条投入稀盐酸中 |
| ⑤ | 将铝条投入稀盐酸中 |
⑴实验目的
⑵写出实验①和②中的实验现象和化学方程式
实验①:现象 化学方程式
实验②:现象 化学方程式
⑶实验结论
查看答案和解析>>
科目:高中化学 来源: 题型:
某溶液只可能含有以下离子中的若干种:H+、NH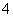 、K+、Mg2+、NO
、K+、Mg2+、NO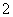 、CO
、CO 、NO
、NO ,现取两份200 mL溶液进行如下实验:(已知HNO2不稳定极易分解2HNO2===H2O+NO2↑+NO↑)
,现取两份200 mL溶液进行如下实验:(已知HNO2不稳定极易分解2HNO2===H2O+NO2↑+NO↑)
①第一份加足量AgNO3溶液后,有11.68 g白色沉淀产生,沉淀中加入足量稀盐酸充分反应,有棕色气体产生,沉淀颜色不变,但是质量减少0.2 g;②将产生的气体全部通入过量的澄清石灰水,又得到白色沉淀2.0 g,该沉淀能溶于稀盐酸产生无色气体;③第二份加入过量浓NaOH溶液,加热使产生的气体全部放出,用100 mL 0.5 mol·L-1的稀硫酸恰好完全吸收,酸也不剩余。
根据上述实验,以下推测不正确的是( )
A.原溶液一定不存在较大浓度的H+、Mg2+
B.原溶液确定含NH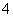 、NO
、NO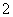 、CO
、CO ,且物质的量之比为5:2:1
,且物质的量之比为5:2:1
C.不能确定原溶液是否含有K+、NO
D.实验中产生的棕色气体遇空气颜色会加深
查看答案和解析>>
科目:高中化学 来源: 题型:
从毒韭菜到炸鸡翅、从速溶茶到儿童奶粉,关于食品质量的报道中不断有①“致癌农药”、②“苏丹红”、③“碘元素”、④“亚硝酸盐”、⑤“三聚氰胺”等化学名词出现。业内人士告诉记者,化学性污染正成为危急食品安全的一大“杀手”。上述化学名词所提到的物质中,在某食品添加剂中允许含有但符合限量时不会引起中毒的是( )
A.②③④ B.②③
C.③④ D.只有③
查看答案和解析>>
科目:高中化学 来源: 题型:
卤素单质的性质活泼,卤素的化合物应用广泛,运用化学反应原理研究卤族元素的有关性质具有重要意义。
(1)下列关于氯水的叙述正确的是________(填写序号)。
A.氯水中存在两种电离平衡
B.向氯水中通入SO2,其漂白性增强
C.向氯水中通入氯气,c(H+)/c(ClO-)减小
D.加水稀释氯水,溶液中的所有离子浓度均减小
E.加水稀释氯水,水的电离平衡向正反应方向移动
F.向氯水中加少量固体NaOH,可能有c(Na+)=c(Cl-)+c(ClO-)
(2)工业上通过氯碱工业生产氯气,其反应的离子方程式为____。
(3)常温下,已知25 ℃时有关弱酸的电离平衡常数:
| 弱酸化学式 | HClO | H2CO3 |
| 电离平衡常数 | K=3.0×10-8 | K1=4.4×10-7,K2=4.7×10-11 |
写出84消毒液(主要成分为NaClO)露置在空气中发生反应的有关化学方程式________________________。若将84消毒液与洁厕剂(含有浓盐酸)混合使用可能会导致中毒,请用离子方程式解释有关原因__________________。
(4)碘钨灯具有比白炽灯寿命长且环保节能的特点。一定温度下,灯内封存的少量碘与使用过程中沉积在管壁上的钨可以发生反应:W(s)+I2(g)WI2(g)。为模拟上述反应,准确称取0.508 g碘、0.736 g金属钨置于50.0 mL的密闭容器中,加热使其反应。
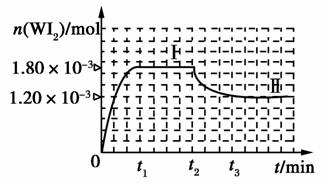
如图是WI2(g)的物质的量随时间变化的关系图像,其中曲线I(0~t2时间段)的反应温度为T1,曲线Ⅱ(从t2开始)的反应温度为T2,且T2>T1。则:
①该反应的ΔH________0(填“>”、“=”或“<”)。
②从反应开始到t1时间内的平均反应速率v(I2)=________。
③下列说法中不正确的是________(填序号)。
A.利用该反应原理可以提纯钨
B.该反应的平衡常数表达式是K=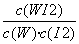
C.灯丝附近温度越高,灯丝附近区域WI2越易变为W而重新沉积到灯丝上
(5)25 ℃时,向5 mL含有KCl和KI浓度均为0.1 mol·L-1的混合液中,滴加6 mL 0.1 mol·L-1的AgNO3溶液,先生成的沉淀是________,溶液中离子浓度由大到小的顺序是________[不考虑H+和OH-。25 ℃时Ksp(AgCl)=1.8×10-10、Ksp(AgI)=8.3×10-17]。
查看答案和解析>>
科目:高中化学 来源: 题型:
室温下向10 mL pH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中 不变
不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10 mL pH=11的NaOH溶液,混合液pH <7
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制取的乙烯常含有少量二氧化硫,现设计如下实验,确认混合气体中有乙烯和二氧化硫。

(1)a、b、c、d装置可盛放的试剂是:a________,b______,c_____,d______。
A.品红溶液 B.NaOH溶液C.浓硫酸 D.酸性高锰酸钾溶液
(2)确定含有乙烯的现象是_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将锌片和铜片用导线连接后平行放入稀硫酸中,发生原电池反应,下列叙述错误的是
A.溶液的pH增大 B.溶液中的Zn2+浓度增大
C.溶液中的SO42— 浓度增大 D.溶液的密度增大
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com