


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:高中化学 来源: 题型:
| A、XW4为非极性分子 |
| B、Y、Z、W的最高价氧化物的水化物酸性强弱顺序是Y<Z<W |
| C、X、Y的氢化物由固态转化为气态时,克服相同的作用力 |
| D、XW4、YW4、ZW2分子中的中心原子均为sp杂化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、乙醇、乙烯都可被酸性高锰酸钾溶液氧化 |
| B、乙烯、苯都可与溴水发生加成反应 |
| C、乙醇、乙酸都可以发生酯化反应 |
| D、淀粉、油脂都可以发生水解反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、新药帕拉米韦对禽流感H7N9有显著疗效,它的结构简式为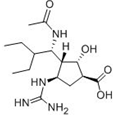 化学式是C15H26N4O4 化学式是C15H26N4O4 |
| B、2013年11月20日山东现‘夺命快递’----化学品泄漏致1死7中毒.该化学品为氟乙酸甲酯它是无色透明液体,溶于乙醇、乙醚,不溶于水.它属于酯类,也属于卤代烃 |
C、绿原酸的结构简式为: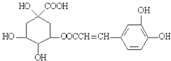 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 ,它在一定条件下能发生氧化、加成、酯化、水解、消去、加聚、缩聚反应 |
D、苯的同系物 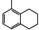 ,其所有碳原子不可能在同一平面上 ,其所有碳原子不可能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:
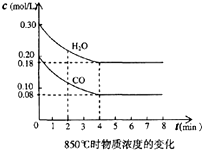 在体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
在体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:查看答案和解析>>
科目:高中化学 来源: 题型:
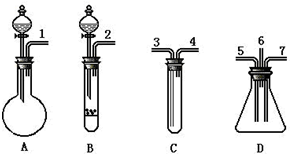 根据下面提供的仪器和试剂,完成验证SO2既有氧化性又有还原性的实验.可选用的仪器如图所示:
根据下面提供的仪器和试剂,完成验证SO2既有氧化性又有还原性的实验.可选用的仪器如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:
A Z |
查看答案和解析>>
科目:高中化学 来源: 题型:
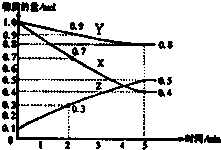 化学反应速率与生产、生活密切相关.
化学反应速率与生产、生活密切相关.| 时间(min) | 1 | 2 | 3 | 4 | 5 |
| 氢气体积(mL)(标准状况) | 50 | 120 | 232 | 288 | 310 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com