
将14 g铜银合金与足量的一定浓度的硝酸溶液反应,把放出的气体与标准状况下体积为1.12 L的O2混合后再通入水中,恰好全部被吸收,则合金中铜的质量为( )
A.3.2 g B.4.8 g
C.6.4 g D.10.8 g
科目:高中化学 来源: 题型:
结合下图判断,下列叙述不正确的是 (把两容器中电解质溶液连通形成回路)
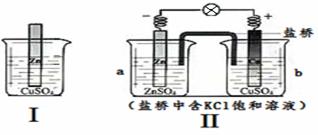
A.Ⅰ、Ⅱ的反应原理均是Zn + Cu2+ = Zn2+ + Cu
B. Ⅰ、Ⅱ中均有电子转移,均是把化学能转化为电能
C. 随着反应的进行,Ⅰ、Ⅱ中CuSO4溶液颜色均渐渐变浅
D. 取a中溶液,加足量Ba(NO3)2溶液,过滤后向滤液中加AgNO3溶液,有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
在含有Cu(NO3)2、Zn(NO3)2、Fe(NO3)3、AgNO3各0.1 mol的混合溶液中加入0.1 mol铁粉,充分搅拌后铁完全反应,溶液中不存在Fe3+,同时析出0.1 mol Ag。则下列结论中不正确的是( )
A.反应后溶液中Cu2+与Fe2+的物质的量之比为1∶2
B.氧化性:Ag+>Fe3+>Cu2+>Zn2+
C.含Fe3+的溶液可腐蚀铜板
D.1 mol Fe可还原3 mol Fe3+
查看答案和解析>>
科目:高中化学 来源: 题型:
化合物A最早发现于酸牛奶中,它是人体内糖代谢的中间体,可由马铃薯、玉米淀粉等发酵制得,A的钙盐是人们喜爱的补钙剂之一。A在某种催化剂的存在下进行氧化,其产物不能发生银镜反应。在浓硫酸存在下,A可发生如下图所示的反应:
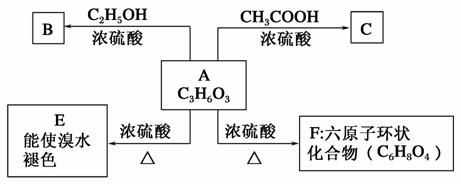
(1)A跟足量金属钠反应的化学方程式为__________________ ______,跟足量Na2CO3溶液反应的化学方程式为________________________。
(2)化合物B、C的结构简式B:________,C:________。
(3)A―→E反应的化学方程式为______________,反应类型____________。
(4)A―→F反应的化学方程式为______________,反应类型____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
铜的冶炼过程大致可分为:
①富集,将硫化物矿进行浮选
②焙烧,主要反应为:
2CuFeS2+4O2===Cu2S+3SO2+2FeO(炉渣)
③制粗铜,在1200℃发生的主要反应为:2Cu2S+3O2===2Cu2O+2SO2;2Cu2O+Cu2S===6Cu+SO2↑
④电解精炼铜
下列说法正确的是( )
A.冶炼过程中的尾气可用来制硫酸
B.上述过程中,由1 mol CuFeS2制取1 mol Cu时共消耗2 mol O2
C.在反应2Cu2O+Cu2S===6Cu+SO2↑中,氧化剂是Cu2O和Cu2S
D.电解精炼铜的过程中,每转移1 mol电子时,阳极溶解铜的质量为32 g
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于生铁和钢的叙述,正确的是( )
A.由铁矿石炼成铁是化学变化,由生铁炼成钢是物理变化
B.用铁制容器盛放硫酸铜溶液,容器易被腐蚀
C.生铁和钢都是铁、碳合金,它们在性能和用途上差别很大
D.它们都能完全溶解在盐酸中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关物质水解的说法正确的是( )
A.蛋白质水解的最终产物是多肽
B.淀粉水解的最终产物是葡萄糖
C.纤维素不能水解成葡萄糖
D.油脂水解产物之一是甘油
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com