
下列叙述正确的是( )
|
| A. | 1mol任何气体的体积一定是22.4L |
|
| B. | 标准状况下,22.4L任何气体所含分子数都约为6.02×1023个 |
|
| C. | 在标准状况下,体积为22.4L的物质都是1mol |
|
| D. | 在非标准状况下,1mol任何气体的体积不可能是22.4L |
| 阿伏加德罗常数;气体摩尔体积. | |
| 专题: | 阿伏加德罗常数和阿伏加德罗定律. |
| 分析: | A.1mol气体必须是标准状况下,气体的体积约为22.4L; B.标准状况下,22.4L任何气体为1mol; C.在标准状况下,体积为22.4L的气体为1mol; D.体积的大小是由压强和温度决定; |
| 解答: | 解:A.决定1mol气体体积大小的因素是气体分子间的平均距离,分子间的平均距离由温度和压强决定,所以,当1mol气体在标准状况下,气体的体积约为22.4L,故A错误; B.1mol分子数约为6.02×1023个,标准状况下,22.4L任何气体的物质的量为1mol,故B正确; C.0°C,1个标准大气压,气体的体积是22.4L,在标准状况下,体积为22.4L的液体和固体的物质的量不为1mol,故C错误; D.0°C,1个标准大气压,气体的体积是22.4L,温度升高,气体将会受热膨胀,体积将会变大,如果在加压,把气体进行压缩,就有可能压缩到22.4升,故D错误; 故选B. |
| 点评: | 本题考查了阿伏伽德罗常数的应用,主要考查气体摩尔体积的条件应用,题目较简单. |


科目:高中化学 来源: 题型:
下列说法不正确的是( )
|
| A. | H2O的沸点比H2S的沸点高是因为O的非金属性比S的非金属性强 |
|
| B. | F2、Cl2、Br2、I2的沸点依次升高是因为它们分子间作用力依次增大 |
|
| C. | 离子化合物溶于水时离子键被破坏,共价化合物溶于水时共价键不一定改变 |
|
| D. | 只含共价键的物质不一定属于共价化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
在一个密闭容器中,盛有N2和H2,它们的起始浓度分别是1.8 mol·L-1和
5.4 mol·L-1,在一定条件下它们反应生成NH3,10 min后测得N2的浓度是
0.8 mol·L-1,则在这10 min内NH3的平均反应速率是( )
A.0.1 mol·L-1·min-1 B.0.3 mol·L-1·min-1
C.0.2 mol·L-1·min-1 D.0.6 mol·L-1·min-1
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,不属于四种基本反应类型是( )
|
| A. | 2Na+2H2O═2NaOH+H2↑ | B. | 2HClO═2HCl+O2↑ |
|
| C. | Fe+2FeCl3═3FeCl2 | D. | CuO+CO |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是( )
|
| A. | 铁与稀硫酸反应:2Fe+6H+=2Fe3﹢+3H2↑ |
|
| B. | Al(OH)3沉淀中滴加盐酸:Al(OH)3+H﹢=Al3﹢+H2O |
|
| C. | 碳酸氢钠溶液中加入氢氧化钠:HCO3﹣+OH﹣=CO32﹣+H2O |
|
| D. | 碳酸钙与稀硝酸反应:CO32﹣+2H+=CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
向含有下列离子的溶液中分别加入烧碱固体(溶液体积变化可忽略),能引起离子浓度减小的是( )
|
| A. | CO32﹣ | B. | Cl﹣ | C. | OH﹣ | D. | Cu2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
配制500mL 0.5mol•L﹣1的NaOH溶液,试回答下列问题:
(1)计算:需要NaOH固体的质量为 g .
(2)某学生用托盘天平称量一个小烧杯的质量,称量前把游码放的标尺的零刻度处,天平静止时发现指针在分度盘的偏右位置,此时左边的托盘将 (填“高于”或“低于”)右边的托盘,欲使天平平衡,所进行的操作为 .假定最终称得小烧杯的质量为 (填“32.6g”或“32.61 g”).
(3)配制方法:设计五个操作步骤
①向盛有NaOH的烧杯中加入200 mL 蒸馏水使其溶解,并冷却至室温.
②继续往容量瓶中加蒸馏水至液面接近刻度线1 cm~2 cm.
③将NaOH溶液沿玻璃棒注入500 mL容量瓶中
④在烧杯中加入少量的蒸馏水,小心洗涤2~3次后移入容量瓶
⑤改用胶头滴管加蒸馏水至刻度线,加盖摇匀.
试将以上操作按正确顺序编出序号 .
(4)某学生实际配制NaOH溶液的浓度0.48mol•L﹣1,原因可能是
A. 使用滤纸称量氢氧化钠固体 B. 容量瓶中原来存有少量蒸馏水
C. 溶解后的烧杯未经多次洗涤 D.定容时仰视刻度.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质进行一氯取代反应后,只能生成四种沸点不同产物的烃是( )
|
| A. | (CH3)2CHCH2CH2CH3 | B. | (CH3CH2)2CHCH3 |
|
| C. | (CH3)2CHCH(CH3)2 | D. | (CH3)3CCH2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
依据氧化还原反应:2Ag+(aq)+Cu(s) Cu2+(aq)+2Ag(s),设计的原电池如图所示。下列有关说法中错误的是 ( )
Cu2+(aq)+2Ag(s),设计的原电池如图所示。下列有关说法中错误的是 ( )
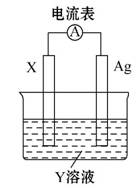
A.电解质溶液Y是CuSO4溶液
B.电极X的材料是Cu
C.银电极为电池的正极,其电极反应为Ag++e-====Ag
D.外电路中的电子是从X电极流向Ag电极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com