
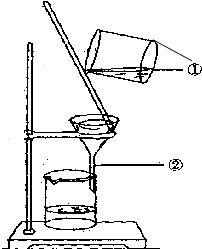
 如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:
如图为某学生进行粗盐提纯实验中过滤操作的示意图,试回答:分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据过滤操作的注意事项分析即可,过滤操作要遵循“一贴”“二低”“三靠”的 原则,
一贴:湿润的滤纸紧贴漏斗内壁.
二低:滤纸低于漏斗边缘,滤液低于滤纸边缘.
三靠:烧杯紧靠玻璃棒,玻璃棒靠在三层滤纸上,漏斗尖嘴紧靠烧杯内壁.
(3)根据玻璃棒的作用和蒸发时的实验操作进行分析;
(4)根据精盐的产率的计算方法进行分析.
解答 解:(1)通过分析图中所指仪器可知,①是烧杯,②是漏斗;故答案为:烧杯;漏斗;
(2)过滤时玻璃棒起引流作用,玻璃棒靠三层滤纸,漏斗中液体的液面应该低于滤纸的边缘;故答案为:玻璃棒,三,滤纸;
(3)蒸发滤液时,用玻璃棒不断搅拌的目的是防止液体受热不匀而飞溅;等到蒸发皿中出现较较多固体时,停止加热,但要用玻璃棒继续搅拌,利用蒸发皿的余热使滤液蒸干,移去蒸发皿时所使用的仪器是坩埚钳;故答案为:防止液体受热不匀而飞溅;较多固体,搅拌,坩埚钳;
(4)精盐的产率=$\frac{5g}{6g}$×100%=83.3%;故答案为:83.3%.
点评 对于过滤操作,很多同学都掌握的差不多,但完全掌握过滤的方方面面,很多同学做不到.这就需要同学们在以后的学习过程中,多总结,理解性的去记忆.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
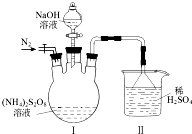
| 实验编号 | 操作 | 现象及结论 |
| a | 加入2mL蒸馏水,再加入10mL 5mol/L Na2S2O8溶液,振荡 | 红色固体逐渐溶解,先慢后快. |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若单位时间生成xmolNO的同时,消耗1.5xmolH2O,则反应达到平衡状态 | |
| B. | 达到平衡状态后,NH3、O2、NO、H2O(g)的物质的量之比为4:5:4:6 | |
| C. | 达到平衡状态时,若增加容器体积,则反应速率增大 | |
| D. | 达到平衡时,5v正(O2)=4v逆(NO) |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
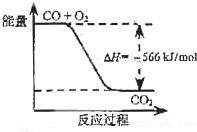 已知:2CO(g)+O2(g)?2CO2(g)△H=-566kJ/mol;
已知:2CO(g)+O2(g)?2CO2(g)△H=-566kJ/mol;| A. | CO(g)与Na2O2(s)反应放出509kJ热量时,消耗的CO是28g | |
| B. | 如图可表示由CO生成CO2的反应过程和能量关系 | |
| C. | 2Na2O2(s)+2CO2(s)═2Na2CO3(s)+O2(g)△H>-452 kJ/mol | |
| D. | CO的燃烧热为-566 kJ/mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 实验I | 实验II | 实验III | |
| 反应温度/℃ | 800 | 800 | 850 |
| c( A)起始/mol•L-1 | 1 | 2 | 1 |
| c( A)平衡/mol•L-1 | 0.5 | 1 | 0.85 |
| 放出的热量/kJ | a | b | c |
| A. | 化学平衡常数实验III的小于实验I的 | |
| B. | 实验放出的热量关系为b>2a | |
| C. | 实验III 在30min达到平衡,用A表示此段时间的平均反应速率v (A)为0.005mol•L-1•min-1 | |
| D. | 当容器内气体密度不随时间而变化时上述反应已达平衡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 任何化学反应都伴随着能量的变化 | |
| B. | 升高温度或加入催化剂,可以改变化学反应的反应热 | |
| C. | 化学反应中的能量变化都是以热量的形式体现 | |
| D. | 2CO(g)+O2(g)═2CO2(g)△H<0,则56g CO和32g O2所具有的总能量小于88g CO2所具有的总能量 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com