
某化学科研小组研究在其他条件不变时,改变某一条件对可逆反应aA(g)+bB(g)  cC(g)化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,
cC(g)化学平衡的影响,得到如下图象(图中p表示压强,T表示温度,n表示物质的量,α表示平衡转化率,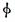 表示体积分数)。根据图象,下列判断正确的是( )
表示体积分数)。根据图象,下列判断正确的是( )
A.反应Ⅰ:若p1>p2,则此反应只能在高温下自发进行
B.反应Ⅱ:此反应的ΔH<0,且T1<T2
C.反应Ⅲ:ΔH>0且T2>T1或ΔH<0且T2<T1
D.反应Ⅳ:T1<T2,则该反应不易自发进行
科目:高中化学 来源: 题型:
下列各组离子或分子在溶液中能大量共存,且满足相应要求的是( )
| 选项 | 离子或分子 | 要求 |
| A | K+、NO | c(K+)<c(Cl-) |
| B | Fe3+、NO | 逐滴滴加盐酸立即有气体产生 |
| C | Na+、HCO | 逐滴滴加氨水立即有沉淀产生 |
| D | NH | 滴加NaOH浓溶液立刻有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
某化学兴趣小组在课外活动中,对某一份溶液成分(已知不含其他还原性离子)进行了检测,其中三次检测结果如表所示:
| 检测序号 | 溶液中检测出的电解质溶液组合 |
| 第一次 | KCl、K2SO4、Na2CO3、NaCl |
| 第二次 | KCl、AlCl3、Na2SO4、K2CO3 |
| 第三次 | Na2SO4、KCl、K2CO3、NaCl |
则下列说法合理的是( )
A.三次检测结果都正确
B.该溶液中的阳离子无法判断
C.为了检验是否存在SO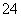 ,应先加过量稀硝酸后再滴加Ba(NO3)2溶液,观察是否有沉淀产生
,应先加过量稀硝酸后再滴加Ba(NO3)2溶液,观察是否有沉淀产生
D.为了检验是否存在CO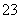 ,可以向溶液中滴加CaCl2溶液,观察是否有沉淀产生
,可以向溶液中滴加CaCl2溶液,观察是否有沉淀产生
查看答案和解析>>
科目:高中化学 来源: 题型:
在恒容密闭容器中A(g)+3B(g)  2C(g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中不正确的是( )
2C(g) ΔH<0,达平衡后,将气体混合物的温度降低,下列叙述中不正确的是( )
A.混合气体密度的变化情况不可以作为判断反应是否再次达平衡的依据
B.容器中混合气体的平均相对分子质量增大
C.正反应速率和逆反应速率都变小,C的百分含量增加
D.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
某密闭容器中进行如下反应:2X(g)+Y(g)⇌2Z(g),若要使平衡时反应物总物质的量与生成物的总物质的量相等,且用X、Y作反应物,则X、Y的初始物质的量之比的范围应满足( )
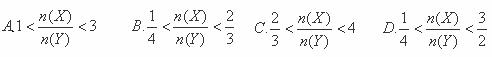
查看答案和解析>>
科目:高中化学 来源: 题型:
在一密闭容器中,反应mM(气) 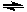 nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则( )
nN(气)达到平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,M的浓度为原来的80%,则( )
A、平衡正向移动; B、物质M的转化率增大; C、n > m D、物质N的质量分数减少
查看答案和解析>>
科目:高中化学 来源: 题型:
下列溶液一定呈中性的是 )。
A.cH+)=cOH-)=10-6 mol·L-1的溶液
B.pH=7的溶液
C.使石蕊试液呈紫色的溶液
D.酸与碱恰好完全反应生成正盐的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
一定条件下,通过下列反应可以制备特种陶瓷的原料MgO:MgSO4s)+COg)MgOs)+CO2g)+SO2g) ΔH>0
该反应在恒容密闭容器中达到平衡后,若仅改变图中横坐标x的值,纵坐标y随x变化趋势合理的是 )。
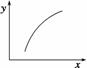
| 选项 | x | y |
| A | 反应时间 | CO2与CO的物质的量之比 |
| B | 反应温度 | 逆反应速率 |
| C | 体系压强 | 平衡常数K |
| D | MgSO4的质量 | CO的转化率 |
查看答案和解析>>
科目:高中化学 来源: 题型:
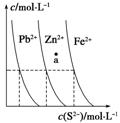 如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况。下列说法正确的是( )
如图为某温度下,PbS(s)、ZnS(s)、FeS(s)分别在溶液中达到沉淀溶解平衡后,溶液的S2-浓度、金属阳离子浓度变化情况。下列说法正确的是( )
A.三种难溶物的溶度积Ksp(FeS)的最小
B.如果向三种沉淀中加盐酸,最先溶解的是PbS
C.向新生成的ZnS浊液中滴入足量含相同浓度的Pb2+、Fe2+的溶液,振荡后,ZnS沉淀会转化为PbS沉淀
D.对于三种难溶物来讲,a点对应的都是不饱和溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com